MINI ການທົບທວນຄືນ
ສະຖານທີ່ຕ້ານມະເຮັງ: ມະເຮັງທົ່ວໄປເທົ່ານັ້ນ
Chengchen Qian1, Xiaolong Zou2, Wei Li1,3, Yinshan Li4, Wenqiang Yu5
1Shanghai Epiprobe Biotechnology Co., Ltd, Shanghai 200233, ຈີນ;2 ພະແນກຜ່າຕັດທົ່ວໄປ, ໂຮງຫມໍຮ່ວມທໍາອິດຂອງມະຫາວິທະຍາໄລການແພດ Harbin, Harbin 150001, ຈີນ;3Shandong Epiprobe Medical Laboratory Co., Ltd, Heze 274108, ຈີນ;4 ໂຮງຫມໍປະຊາຊົນຂອງເຂດປົກຄອງຕົນເອງ Ningxia Hui, Ningxia ການແພດວິທະຍາໄລ, Yinchuan 750002, ຈີນ;5Shanghai Public Health Clinical Clinical Center & Department of General Surgery, Huashan Hospital & Cancer Metastasis Institute & Laboratory of RNA Epigenetics, Institutes of Biomedical Sciences, Shanghai Medical College, Fudan University, Shanghai 200032, ຈີນ
ບົດຄັດຫຍໍ້
ມະເຮັງແມ່ນສາເຫດອັນດັບຕົ້ນໆຂອງການເສຍຊີວິດໃນທົ່ວໂລກ.ການກວດຫາມະເຮັງໄວສາມາດຫຼຸດອັດຕາການຕາຍຂອງມະເຮັງທຸກປະເພດ;ແນວໃດກໍ່ຕາມ, biomarkers ທີ່ມີປະສິດຕິຜົນໃນການກວດຫາເບື້ອງຕົ້ນແມ່ນຂາດແຄນສໍາລັບມະເຮັງປະເພດສ່ວນໃຫຍ່.DNA methylation ເຄີຍເປັນເປົ້າຫມາຍທີ່ສໍາຄັນຂອງຄວາມສົນໃຈເພາະວ່າ DNA methylation ມັກຈະເກີດຂື້ນກ່ອນການປ່ຽນແປງທາງພັນທຸກໍາທີ່ກວດພົບໄດ້.ໃນຂະນະທີ່ການສືບສວນລັກສະນະທົ່ວໄປຂອງມະເຮັງໂດຍນໍາໃຊ້ຄູ່ມືນະວະນິຍາຍການຈັດລໍາດັບການຈັດລໍາດັບ DNA methylation, ຊຸດຂອງມະເຮັງທົ່ວໄປພຽງແຕ່ເຄື່ອງຫມາຍ (UCOMs) ໄດ້ກາຍເປັນຜູ້ສະຫມັກທີ່ເຂັ້ມແຂງສໍາລັບການກວດພົບມະເຮັງໄວແລະຖືກຕ້ອງ.ໃນຂະນະທີ່ມູນຄ່າທາງດ້ານຄລີນິກຂອງຕົວຊີ້ບອກມະເຮັງໃນປະຈຸບັນແມ່ນຫຼຸດລົງໂດຍຄວາມອ່ອນໄຫວຕ່ໍາແລະ / ຫຼືຄວາມສະເພາະຕ່ໍາ, ຄຸນລັກສະນະທີ່ເປັນເອກະລັກຂອງ UCOMs ຮັບປະກັນຜົນໄດ້ຮັບທີ່ມີຄວາມຫມາຍທາງດ້ານການຊ່ວຍ.ການກວດສອບທ່າແຮງທາງດ້ານຄລີນິກຂອງ UCOMs ໃນມະເຮັງປອດ, ປາກມົດລູກ, endometrial, ແລະ urothelial ຍັງສະຫນັບສະຫນູນການນໍາໃຊ້ UCOMs ໃນຫຼາຍປະເພດມະເຮັງແລະສະຖານະການທາງດ້ານການຊ່ວຍຕ່າງໆ.ໃນຄວາມເປັນຈິງ, ຄໍາຮ້ອງສະຫມັກຂອງ UCOMs ປະຈຸບັນຢູ່ພາຍໃຕ້ການສືບສວນຢ່າງຫ້າວຫັນດ້ວຍການປະເມີນຜົນເພີ່ມເຕີມໃນການກວດຫາມະເຮັງເບື້ອງຕົ້ນ, ການບົ່ງມະຕິຊ່ວຍ, ປະສິດທິພາບການປິ່ນປົວ, ແລະການຕິດຕາມການເກີດໃຫມ່.ກົນໄກໂມເລກຸນທີ່ UCOMs ກວດພົບມະເຮັງແມ່ນຫົວຂໍ້ທີ່ສໍາຄັນຕໍ່ໄປທີ່ຈະສືບສວນ.ຄໍາຮ້ອງສະຫມັກຂອງ UCOMs ໃນສະຖານະການທີ່ແທ້ຈິງຍັງຮຽກຮ້ອງໃຫ້ມີການປະຕິບັດແລະການປັບປຸງໃຫມ່.
ຄີເວີດ
ການກວດຫາມະເຮັງ;ການກວດຫາມະເຮັງ;DNA methylation;epigenetics ມະເຮັງ;biomarkers ມະເຮັງ
ເປັນຫຍັງພວກເຮົາຕ້ອງການອັນໃໝ່ດ່ວນ ເຄື່ອງຫມາຍຊີວະພາບ?
ຫຼັງຈາກການຕ້ານມະເຮັງເປັນເວລາຫຼາຍກວ່າສັດຕະວັດ, ມະເຮັງຍັງເປັນໄພຂົ່ມຂູ່ທາງຊີວະພາບທີ່ສຸດຂອງມະນຸດຊາດ.ມະເຮັງຍັງຄົງເປັນຄວາມກັງວົນດ້ານສຸຂະພາບທົ່ວໂລກ ໂດຍມີຜູ້ຕິດເຊື້ອໃໝ່ 19.3 ລ້ານຄົນ ແລະ ເກືອບ 10 ລ້ານຄົນເສຍຊີວິດໃນປີ 20201. ໃນປີ 2020 ຄາດຄະເນວ່າມີກໍລະນີມະເຮັງໃໝ່ 4.6 ລ້ານຄົນຖືກກວດພົບໃນປະເທດຈີນ, ກວມເອົາ 23.7% ຂອງກໍລະນີມະເຮັງໃໝ່ໃນທົ່ວໂລກ ອີງຕາມ GLOBOCAN1.ນອກຈາກນັ້ນ, ປະມານ 3 ລ້ານຄົນເສຍຊີວິດຍ້ອນມະເຮັງໃນປະເທດຈີນໃນປີ 2020, ເຊິ່ງເປັນ 30% ຂອງການເສຍຊີວິດທີ່ກ່ຽວຂ້ອງກັບມະເຮັງທົ່ວໂລກ.ສະຖິຕິເຫຼົ່ານີ້ຊີ້ໃຫ້ເຫັນວ່າຈີນເປັນອັນດັບໜຶ່ງໃນການເກີດແລະອັດຕາການຕາຍຂອງພະຍາດມະເຮັງ.ຍິ່ງໄປກວ່ານັ້ນ, ອັດຕາການລອດຊີວິດຂອງມະເຮັງ 5 ປີແມ່ນ 40.5%, ເຊິ່ງແມ່ນ 1.5 ເທົ່າຂອງອັດຕາການລອດຊີວິດຂອງ 5 ປີໃນສະຫະລັດ2,3.ອັດຕາການຢູ່ລອດທີ່ຕ່ຳກວ່າແລະອັດຕາການຕາຍຂອງຈີນທີ່ສູງກວ່າໃນປະເທດທີ່ມີດັດຊະນີການພັດທະນາມະນຸດສູງນັ້ນ ຊີ້ໃຫ້ເຫັນວ່າລະບົບປ້ອງກັນແລະເຝົ້າລະວັງມະເຮັງທີ່ມີປະສິດທິຜົນແລະຄຸ້ມຄ່າແມ່ນຕ້ອງການຢ່າງຮີບດ່ວນ.ການກວດຫາມະເຮັງກ່ອນໄວອັນຄວນແມ່ນໜຶ່ງໃນອົງປະກອບທີ່ສຳຄັນທີ່ສຸດໃນລະບົບການດູແລສຸຂະພາບ.ການກວດຫາມະເຮັງໄວສາມາດປັບປຸງການຄາດການແລະການຢູ່ລອດໃນໄລຍະເລີ່ມຕົ້ນຂອງມະເຮັງເກືອບທັງໝົດປະເພດ4.ຍຸດທະສາດການກວດກາທີ່ປະສົບຜົນສໍາເລັດໄດ້ເຮັດໃຫ້ອັດຕາການຕາຍຂອງມະເຮັງປາກມົດລູກ, ເຕົ້ານົມ, ລໍາໄສ້ໃຫຍ່, ແລະຕ່ອມລູກຫມາກຫຼຸດລົງຢ່າງຫຼວງຫຼາຍ.
ຢ່າງໃດກໍຕາມ, ເພື່ອບັນລຸການກວດພົບມະເຮັງໄວ, ບໍ່ແມ່ນວຽກທີ່ງ່າຍ.ການສືບສວນຊີວະວິທະຍາແລະການຄາດຄະເນຂອງມະເຮັງຕົ້ນ, ການກໍານົດແລະການກວດສອບ bio-markers ການກວດສອບເບື້ອງຕົ້ນທີ່ເຊື່ອຖືໄດ້, ແລະການພັດທະນາເຕັກໂນໂລຊີການກວດຫາເບື້ອງຕົ້ນທີ່ສາມາດເຂົ້າເຖິງໄດ້ແລະຖືກຕ້ອງແມ່ນສະເຫມີເປັນອຸປະສັກທີ່ຍິ່ງໃຫຍ່ທີ່ສຸດໃນຂະບວນການ4.ການກວດຫາມະເຮັງທີ່ຊັດເຈນສາມາດຈໍາແນກ benign ຈາກ lesions malignant, ເຊິ່ງຊ່ວຍຫຼີກເວັ້ນການຂັ້ນຕອນທີ່ບໍ່ຈໍາເປັນແລະອໍານວຍຄວາມສະດວກໃນການຄຸ້ມຄອງພະຍາດຕື່ມອີກ.ຍຸດທະສາດການກວດຫາເບື້ອງຕົ້ນໃນປະຈຸບັນລວມມີການກວດ biopsies ໂດຍອີງໃສ່ endoscope, ການຖ່າຍຮູບທາງການແພດ, cytology, immunoassays, ແລະ biomarker tests5-7.ເປັນການລົບກວນ ແລະ ຄ່າໃຊ້ຈ່າຍ, ການກວດ biopsies ໂດຍອີງໃສ່ endoscope ມີພາລະອັນຫນັກຫນ່ວງໂດຍພື້ນຖານແລ້ວເປັນຂັ້ນຕອນທາງການແພດທີ່ສໍາຄັນໂດຍອີງໃສ່ບຸກຄະລາກອນມືອາຊີບ.ເຊັ່ນດຽວກັນກັບ cytology, ທັງສອງວິທີການກວດແມ່ນຂຶ້ນກັບຜູ້ຊ່ຽວຊານດ້ານການແພດແລະອີງໃສ່ການຕັດສິນສ່ວນບຸກຄົນທີ່ມີການປະຕິບັດທີ່ໄກຈາກ 8 ທີ່ເຫມາະສົມ.ໃນທາງກົງກັນຂ້າມ, immunoassays ແມ່ນບໍ່ຖືກຕ້ອງສູງ, ເນື່ອງຈາກອັດຕາທີ່ບໍ່ຖືກຕ້ອງສູງ.ການຖ່າຍຮູບທາງການແພດ, ເປັນກົນລະຍຸດການກວດ, ຕ້ອງການອຸປະກອນລາຄາແພງແລະນັກວິຊາການພິເສດ.ດັ່ງນັ້ນ, ການຖ່າຍຮູບທາງການແພດແມ່ນຈໍາກັດທີ່ສຸດເນື່ອງຈາກການເຂົ້າເຖິງຕ່ໍາ.ສໍາລັບເຫດຜົນທັງຫມົດເຫຼົ່ານີ້, biomarkers ເບິ່ງຄືວ່າເປັນທາງເລືອກທີ່ດີກວ່າສໍາລັບການກວດພົບມະເຮັງໄວ.
ສື່ສານກັບ: Yinshan Li ແລະ Wenqiang Yu
Email: liyinshan@nxrmyy.com and wenqiangyu@fudan.edu.cn
ORCID ID: https://orcid.org/0009-0005-3340-6802 ແລະ
https://orcid.org/0000-0001-9920-1133
ໄດ້ຮັບວັນທີ 22 ສິງຫາ 2023;ຍອມຮັບໃນວັນທີ 12 ຕຸລາ 2023;
ຈັດພີມມາອອນໄລນ໌ໃນວັນທີ 28 ພະຈິກ 2023.
ມີຢູ່ www.cancerbiomed.org
©2023 ຊີວະວິທະຍາມະເຮັງ ແລະຢາ.Creative Commons
ໃບອະນຸຍາດສາກົນ Attribution-NonCommercial 4.0
Biomarkers ປະຈຸບັນໄດ້ຖືກຈັດປະເພດເປັນທາດໂປຼຕີນ, ເຄື່ອງຫມາຍການກາຍພັນຂອງ DNA, ເຄື່ອງຫມາຍການແຜ່ກະຈາຍພັນທຸກໍາ, ຄວາມຜິດປົກກະຕິຂອງໂຄໂມໂຊມ, ເຄື່ອງຫມາຍ RNA ທີ່ມາຈາກເນື້ອງອກໂດຍກົງ, ຫຼືຊິ້ນເນື້ອງອກທີ່ໄດ້ຮັບໂດຍທາງອ້ອມຈາກນ້ໍາຂອງຮ່າງກາຍ.ເຄື່ອງໝາຍທາດໂປຼຕີນແມ່ນເຄື່ອງໝາຍຊີວະພາບທີ່ນຳໃຊ້ຢ່າງກວ້າງຂວາງທີ່ສຸດໃນການກວດ ແລະວິນິດໄສມະເຮັງ.ເຄື່ອງຫມາຍຊີວະພາບຂອງທາດໂປຼຕີນ, ເປັນຕົວຊີ້ບອກທາງຊີວະພາບ, ແມ່ນຖືກຈໍາກັດໂດຍແນວໂນ້ມທີ່ໄດ້ຮັບຜົນກະທົບຈາກ lesions benign, ເຊິ່ງນໍາໄປສູ່ການວິນິດໄສແລະການປິ່ນປົວເກີນ, ດັ່ງທີ່ໄດ້ລາຍງານມາສໍາລັບ α-fetoprotein ແລະ prostate-specific antigen (PSA)9,10.ເຄື່ອງຫມາຍ RNA ປະກອບມີຮູບແບບການສະແດງອອກທາງພັນທຸກໍາແລະເຄື່ອງຫມາຍ RNA ທີ່ບໍ່ແມ່ນລະຫັດອື່ນໆ. ການປະສົມປະສານຂອງເຄື່ອງຫມາຍ RNA ການສະແດງອອກທາງພັນທຸກໍາສາມາດກວດພົບໄດ້ໂດຍໃຊ້ຕົວຢ່າງນໍ້າປັດສະວະ, ຄວາມອ່ອນໄຫວຂອງທີ່ຫ່າງໄກຈາກຄວາມພໍໃຈ (60%) ສໍາລັບເນື້ອງອກຕົ້ນຕໍ, ແລະການກວດພົບທີ່ສາມາດ ໄດ້ຮັບຜົນກະທົບຈາກລັກສະນະການຍ່ອຍສະຫຼາຍຂອງ RNA ໃນສະພາບແວດລ້ອມປົກກະຕິ11.ເຄື່ອງຫມາຍພັນທຸກໍາແລະ epigenetic ທັງສອງປະເຊີນກັບບັນຫາຂອງອັດຕາການແຜ່ກະຈາຍຂອງ tumor ແລະການຈໍາກັດຂອງປະເພດມະເຮັງ.
DNA methylation ໄດ້ເປັນຜູ້ສະຫມັກທີ່ເຂັ້ມແຂງເປັນ biomarker ການກວດຫາເບື້ອງຕົ້ນນັບຕັ້ງແຕ່ໄດ້ຖືກເຊື່ອມຕໍ່ຄັ້ງທໍາອິດກັບມະເຮັງໂດຍ Feinberg ໃນປີ 198312. DNA methylation aberrations ແມ່ນສັງເກດເຫັນຢູ່ໃນທຸກຂັ້ນຕອນຂອງມະເຮັງ, ໃນໄລຍະເລີ່ມຕົ້ນຂອງ precancerous.hypermethylation DNA ທີ່ຜິດປົກກະຕິມັກຈະເກີດຂຶ້ນຢູ່ໃນເກາະ CpG ໃນຕົວສົ່ງເສີມພັນທຸກໍາເພື່ອຕ້ານການສະກັດກັ້ນ tumor13,14.ການສຶກສາຍັງໄດ້ແນະນໍາວ່າ hypermethylation DNA ຜິດປົກກະຕິມີສ່ວນຮ່ວມໃນການປັບປຸງລະບົບການຄວບຄຸມທາງເລືອກ 15.ຮ່ອມພູ DNA methylation, ເຊິ່ງມັກຈະກ່ຽວຂ້ອງກັບຜູ້ຄວບຄຸມການພັດທະນາແລະມະເຮັງ hypermethylated, ອາດຈະປ່ຽນຮູບແບບການສະແດງອອກຂອງ gene ໄປສູ່ໂຫມດ DNA methylation-dependent ທີ່ຫມັ້ນຄົງຫຼາຍແລະຫຼຸດລົງການເຊື່ອມຕໍ່ກັບ methylated histone H3K27me3 ແລະທາດໂປຼຕີນຈາກ polycomb ທີ່ກ່ຽວຂ້ອງ 16,17.
ໃນບັນດາຈໍານວນຂະຫນາດໃຫຍ່ຂອງເຄື່ອງຫມາຍ methylation DNA ທີ່ຈັດພີມມາ, ຫຼາຍໆຄົນໄດ້ເປີດຕົວຢ່າງປະສົບຜົນສໍາເລັດໃນຕະຫຼາດ;ແນວໃດກໍ່ຕາມ, ເຄື່ອງໝາຍ DNA methylation ທີ່ເປັນການຄ້າໃນປະຈຸບັນ ແລະ ແຜງວິນິດໄສຍັງບໍ່ທັນໄດ້ປົດລັອກທ່າແຮງຂອງການກວດຫາມະເຮັງໃນໄວກ່ອນໄວອັນຄວນດ້ວຍເຫດຜົນຫຼາຍຢ່າງ 18.ໃນຂະນະທີ່ສ່ວນໃຫຍ່ແມ່ນສະແດງໃຫ້ເຫັນການປະຕິບັດທີ່ຍອມຮັບໄດ້ໂດຍນໍາໃຊ້ຂໍ້ມູນຖານຂໍ້ມູນ, biomarkers ເຫຼົ່ານີ້ມັກຈະປະຕິບັດຫນ້ອຍຕາມຄວາມເຫມາະສົມໃນໂລກທີ່ແທ້ຈິງເນື່ອງຈາກຄວາມຈິງທີ່ວ່າຕົວຢ່າງໃນໂລກທີ່ແທ້ຈິງມັກຈະສັບສົນຫຼາຍແລະບໍ່ເປັນຕົວແທນທີ່ເລືອກຢູ່ໃນຖານຂໍ້ມູນ.ການກວດຫາໂຣກ methylation ໃນໄລຍະຕົ້ນຂອງມະເຮັງຫຼາຍຊະນິດຕາມລຳດັບຕໍ່ໆໄປໄດ້ສະແດງໃຫ້ເຫັນວ່າມີຄວາມອ່ອນໄຫວພຽງແຕ່ 16.8% ແລະ 40.4% ໃນມະເຮັງໄລຍະ I ແລະ II, ຕາມລໍາດັບ19.ການທົດສອບການກວດຫາເບື້ອງຕົ້ນຕ້ອງການຄວາມໝັ້ນຄົງຫຼາຍຂື້ນ ແລະຕົວໝາຍຊີວະພາບທີ່ຖືກຕ້ອງກວ່າ.
ການຄົ້ນພົບຕົວຊີ້ບອກມະເຮັງທົ່ວໄປ (UCOM) ໂດຍໃຊ້ການຈັດລຳດັບຕຳແໜ່ງຄູ່ມື (GPS)
ເຖິງວ່າຈະມີການຄົ້ນຄວ້າມະເຮັງຫຼາຍທົດສະວັດ, ການປ້ອງກັນແລະການປິ່ນປົວທີ່ຫນ້າພໍໃຈຍັງບໍ່ທັນໄດ້ຮັບຮູ້.ວິທີການໃຫມ່ແມ່ນຈໍາເປັນເພື່ອໃຫ້ນັກຄົ້ນຄວ້າສາມາດປະເມີນມະເຮັງຢ່າງລະອຽດ.ໃນໄລຍະ 23 ປີທີ່ຜ່ານມາ, 6 ລັກສະນະທີ່ເປັນມະເຮັງ, ເຊັ່ນ: ການຫຼີກລ່ຽງການເປັນໂຣກ apoptosis, ການບຸກລຸກຂອງເນື້ອເຍື່ອ & ການແຜ່ກະຈາຍ, ແລະອື່ນໆ, ໄດ້ຖືກຂະຫຍາຍອອກເປັນ 14 ຢ່າງ, ລວມທັງລັກສະນະຕ່າງໆເຊັ່ນ: ການສືບພັນທາງພັນທຸກໍາທີ່ບໍ່ປ່ຽນແປງ ແລະ microbiomes polymorphic20,21.ໃນຂະນະທີ່ລາຍລະອຽດເພີ່ມເຕີມກ່ຽວກັບມະເຮັງໄດ້ຖືກເປີດເຜີຍ, ທັດສະນະເພີ່ມເຕີມໄດ້ຖືກນໍາສະເຫນີເຂົ້າໃນການຄົ້ນຄວ້າມະເຮັງ.ການຄົ້ນຄວ້າມະເຮັງໄດ້ຄ່ອຍໆເຂົ້າສູ່ຍຸກໃຫມ່ໃນສອງທິດທາງ (ທົ່ວໄປແລະສ່ວນບຸກຄົນ).ດ້ວຍການພັດທະນາຂອງພະຍາດມະເຮັງທີ່ຊັດເຈນໃນຊຸມປີມໍ່ໆມານີ້, ຈຸດສຸມຂອງການຄົ້ນຄວ້າມະເຮັງແມ່ນເອື່ອຍໄປຫາການປິ່ນປົວດ້ວຍເປົ້າຫມາຍສ່ວນບຸກຄົນແລະຄວາມແຕກຕ່າງກັນຂອງມະເຮັງ22.ດັ່ງນັ້ນ, ເມື່ອບໍ່ດົນມານີ້, ຕົວຊີ້ບອກທາງຊີວະພາບຂອງມະເຮັງໄດ້ສຸມໃສ່ຕົ້ນຕໍແມ່ນປະເພດມະເຮັງສະເພາະ, ເຊັ່ນ: PAX6 forcer-vical cancer23 ແລະ BMP3 ສໍາລັບມະເຮັງລໍາໄສ້ໃຫຍ່24.ປະສິດທິພາບຂອງ biomarkers ເຫຼົ່ານີ້ສະເພາະກັບປະເພດມະເຮັງແຕກຕ່າງກັນ, ແຕ່ມັນຍັງເປັນໄປບໍ່ໄດ້ສໍາລັບບຸກຄົນທີ່ມີຄວາມອ່ອນໄຫວຕໍ່ກັບການກວດສອບມະເຮັງທັງຫມົດພ້ອມໆກັນໄດ້ເນື່ອງຈາກຂໍ້ຈໍາກັດຂອງການໄດ້ຮັບຕົວຢ່າງທາງຊີວະພາບແລະຄ່າໃຊ້ຈ່າຍສູງ.ມັນຈະເປັນທີ່ເຫມາະສົມຖ້າພວກເຮົາສາມາດກໍານົດຕົວຊີ້ທາງຊີວະພາບອັນດຽວ, ທີ່ເຂັ້ມແຂງທີ່ມີປະສິດຕິຜົນສໍາລັບມະເຮັງທຸກປະເພດຢູ່ໃນຂັ້ນຕົ້ນ.
ເພື່ອບັນລຸເປົ້າຫມາຍທີ່ເຫມາະສົມດັ່ງກ່າວ, ຜູ້ສະຫມັກ biomarker ທີ່ດີກວ່າຕ້ອງໄດ້ຮັບການຄັດເລືອກຈາກບັນຊີລາຍຊື່ຂອງປະເພດ biomarker ທີ່ເປັນໄປໄດ້.ຄວາມຜິດກະຕິຂອງ DNA methylation, ໃນບັນດາພັນທຸກໍາແລະ epigenet, ເປັນທີ່ຮູ້ຈັກວ່າມີຄວາມກ່ຽວຂ້ອງກັບມະເຮັງແລະເປັນບາງອັນທໍາອິດ, ຖ້າບໍ່ແມ່ນຄັ້ງທໍາອິດ, ຄວາມຜິດປົກກະຕິກ່ຽວກັບມະເຮັງຈະເກີດຂື້ນຕາມລໍາດັບ.ການສືບສວນ DNA methylation ໄດ້ເລີ່ມຕົ້ນແຕ່ຕົ້ນ, ແຕ່ໄດ້ຖືກຂັດຂວາງໂດຍການຂາດວິທີການຄົ້ນຄ້ວາ.ໃນບັນດາ 28 ລ້ານສະຖານທີ່ CpG methylated ທີ່ມີທ່າແຮງໃນ genome, ຈໍານວນທີ່ສາມາດຄຸ້ມຄອງໄດ້ຕ້ອງໄດ້ຮັບການກວດພົບແລະສອດຄ່ອງກັບ genome ເພື່ອເຂົ້າໃຈ tumorigenesis ໄດ້ດີຂຶ້ນ.ການຈັດລໍາດັບ genome bisulfite ທັງຫມົດ (WGBS), ເຊິ່ງຖືວ່າເປັນມາດຕະຖານຄໍາຂອງລໍາດັບ DNA methylation, ສາມາດກວມເອົາພຽງແຕ່ 50% ຂອງ Cs ໃນຈຸລັງມະເຮັງເນື່ອງຈາກລັກສະນະຂອງການປິ່ນປົວ bisulfite ທີ່ທໍາລາຍຊິ້ນ DNA ແລະຫຼຸດລົງຄວາມສັບສົນຂອງ genome ໃນລະຫວ່າງ. ການປ່ຽນແປງຂອງ Cs-to-Ts25.ວິທີການອື່ນໆ, ເຊັ່ນ: ຊິບ 450k, ພຽງແຕ່ກວມເອົາ 1.6% ຂອງ genome methylation.ອີງຕາມຂໍ້ມູນ 450k, ແຜງກວດຫາ DNA methylation ມີຄວາມອ່ອນໄຫວ 35.4% ສໍາລັບ 6 ຊະນິດຂອງມະເຮັງໄລຍະ I 26.ຂໍ້ຈໍາກັດຂອງປະເພດມະເຮັງ, ການປະຕິບັດທີ່ບໍ່ດີ, ແລະສິ່ງລົບກວນທີ່ສ້າງຂຶ້ນໂດຍວິທີການກວດພົບໃນຂະບວນການວິເຄາະໄດ້ກາຍເປັນອຸປະສັກໃຫຍ່ທີ່ສຸດສໍາລັບແຜງກວດຫາໂຣກມະເຮັງ.
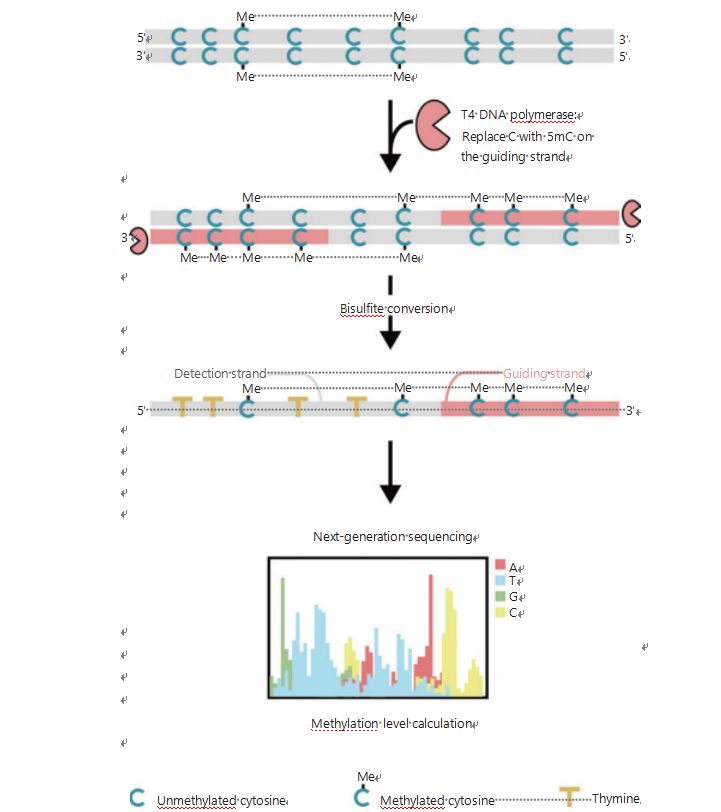
ເພື່ອສືບສວນຮູບແບບ epigenetic ຂອງຈຸລັງທີ່ດີກວ່າໃນໄລຍະ tumorigenesis ແລະ metastasis, ພວກເຮົາໄດ້ພັດທະນາ GPS ທີ່ເປັນເອກະລັກສໍາລັບການກວດພົບ DNA methylation ຂອງ genome, ເຊິ່ງກວມເອົາເຖິງ 96% ຂອງສະຖານທີ່ CpG ໃນ 0.4 ຕື້ reads25.GPS ແມ່ນວິທີການຈັດລໍາດັບແບບ bilateral ໂດຍໃຊ້ຊິ້ນສ່ວນ DNA ຂອງ 3′ ປາຍຂອງ methyl-cytosines ທີ່ບໍ່ປ່ຽນແປງໄດ້ຫຼັງຈາກການປິ່ນປົວ bisulfite ທີ່ນໍາພາການຈັດຕໍາແຫນ່ງຂອງການຄິດໄລ່ DNA methylation ຂອງ 5′ ໃນຕອນທ້າຍໂດຍຜ່ານການຈັດລໍາດັບຄູ່ (ຮູບ 1) 25.ເສັ້ນນໍາທາງ methyl-cytosine, ເຮັດຫນ້າທີ່ເປັນສາຍແມ່ແບບ, ຊ່ວຍໃນການຈັດລໍາດັບພາກພື້ນ GC ສູງທີ່ຟື້ນຕົວຂໍ້ມູນລໍາດັບທີ່ຖືກປະຖິ້ມຫຼາຍທີ່ສຸດໃນ WGBS ແບບດັ້ງເດີມ.ຄຸນສົມບັດການຄອບຄຸມສູງຂອງ GPS ສະຫນອງຂໍ້ມູນ DNA methylation ຈໍານວນຫຼວງຫຼາຍ, ເຊິ່ງຊ່ວຍໃຫ້ພວກເຮົາສາມາດກວດເບິ່ງໂປຣໄຟລ໌ methylation ມະເຮັງທີ່ມີຄວາມລະອຽດສູງກວ່າຢ່າງຫຼວງຫຼາຍໃນພາກພື້ນທີ່ບໍ່ໄດ້ຮັບການສືບສວນກ່ອນຫນ້ານີ້.
GPS ໃຫ້ພວກເຮົາມີເຄື່ອງມືທີ່ມີປະສິດທິພາບໃນການສືບສວນຄວາມຄ້າຍຄືກັນຂອງມະເຮັງ, ເຊິ່ງສາມາດເຮັດໃຫ້ການຄົ້ນຄວ້າມະເຮັງງ່າຍຫຼາຍແລະສາມາດຊອກຫາຄໍາອະທິບາຍທົ່ວໄປສໍາລັບ tum-origenesis ແລະ metastasis.ໃນຂະນະທີ່ການວິເຄາະຂໍ້ມູນ GPS ຂອງສາຍມະເຮັງ, ປະກົດການທີ່ເປັນເອກະລັກໄດ້ພົບເລື້ອຍໆ.ມີຫຼາຍຂົງເຂດທີ່ປະກົດວ່າມີ hypermethylated ຜິດປົກກະຕິໃນຫຼາຍຊະນິດຂອງຕົວຢ່າງມະເຮັງ.ການຄົ້ນພົບທີ່ບໍ່ຄາດຄິດນີ້ໄດ້ຖືກກວດສອບຕໍ່ມາເພື່ອຮັບໃຊ້ເປັນ UCOMs.ຕົວຢ່າງຫຼາຍກວ່າ 7,000 ຕົວຢ່າງຈາກ 17 ຊະນິດຂອງມະເຮັງໃນຖານຂໍ້ມູນ The Cancer Genome Atlas (TCGA) ໄດ້ຖືກວິເຄາະ, ໃນນັ້ນພວກເຮົາໄດ້ກໍານົດ UCOM ທໍາອິດ, HIST1H4F, gene ທີ່ກ່ຽວຂ້ອງກັບ histone ທີ່ມີ hypermethylated ໃນທຸກປະເພດຂອງມະເຮັງ27.ຫຼັງຈາກນັ້ນ, ຊຸດ UCOMs ໄດ້ຖືກພົບເຫັນແລະກວດສອບຢູ່ໃນຖານຂໍ້ມູນ TCGA, ຖານຂໍ້ມູນ Gene Expression Omnibus (GEO), ແລະຕົວຢ່າງທາງດ້ານຄລີນິກໃນໂລກທີ່ແທ້ຈິງ.ໃນປັດຈຸບັນ, HIST1H4F, PCDHGB7, ແລະ SIX6 ໄດ້ຖືກພົບເຫັນແລະຖືກກວດສອບວ່າເປັນ UCOMs.ການຄົ້ນພົບທີ່ບໍ່ຄາດຄິດຂອງ UCOMs ສະຫນອງຄໍາຕອບທີ່ມີປະສິດທິພາບຕໍ່ຄວາມຕ້ອງການສໍາລັບການກວດພົບມະເຮັງໄວ.UCOMs ສະຫນອງການແກ້ໄຂສໍາລັບການກວດພົບເຄື່ອງຫມາຍດຽວຂອງມະເຮັງຫຼາຍຊະນິດ.
ຄຸນລັກສະນະຂອງ UCOMs
ເມື່ອການກວດສອບຄວາມຖືກຕ້ອງ, UCOMs ໄດ້ຖືກສະແດງໃຫ້ເຫັນເຖິງສີ່ລັກສະນະທີ່ສໍາຄັນທີ່ເຮັດໃຫ້ UCOMs ສາມາດລື່ນກາຍປະສິດທິພາບຂອງ biomarkers ໃນປະຈຸບັນ (ຮູບ 2).
ເປັນເອກະລັກຂອງ malignancy
UCOMs ແມ່ນເປັນເອກະລັກຂອງ lesions ມະເຮັງຫຼືກ່ອນເປັນມະເຮັງແລະບໍ່ໄດ້ຮັບຜົນກະທົບຈາກການປ່ຽນແປງທາງກາຍະພາບປົກກະຕິ.ບາງເຄື່ອງໝາຍທີ່ກ່ຽວຂ້ອງກັບມະເຮັງໃນປະຈຸບັນທີ່ໄດ້ຖືກນຳໃຊ້ຢ່າງກວ້າງຂວາງໃນການກວດຫາ ແລະ/ຫຼື ການກວດຫາເບື້ອງຕົ້ນໄດ້ນຳໄປສູ່ການວິນິດໄສຫຼາຍເກີນໄປ.ລະດັບ PSA ສູງ, ເປັນເຄື່ອງມືກວດຫາທາງຄລີນິກ, ຍັງຖືກກວດພົບໃນສະພາບທີ່ອ່ອນເພຍ, ເຊັ່ນ: ຕ່ອມລູກໝາກ ແລະ prostatitis10.ການວິນິດໄສ ແລະ ການປິ່ນປົວເກີນຜົນເຮັດໃຫ້ຄຸນນະພາບຊີວິດຫຼຸດລົງຍ້ອນການລຳໄສ້, ຍ່ຽວ ແລະ ອາການແຊກຊ້ອນທາງເພດ28.ເຄື່ອງຫມາຍຊີວະພາບທີ່ມີທາດໂປຼຕີນອື່ນໆແລະຖືກນໍາໃຊ້ຢ່າງກວ້າງຂວາງໃນສະຖານທີ່ທາງດ້ານຄລີນິກ, ເຊັ່ນ CA-125, ບໍ່ໄດ້ຮັບຜົນປະໂຫຍດທີ່ສໍາຄັນໃນຂະນະທີ່ເກີດການວິນິດໄສຫຼາຍເກີນໄປແລະການປິ່ນປົວເກີນ 29.ຄວາມສະເພາະເຈາະຈົງສູງຂອງ UCOMs ສໍາລັບ malignancies ຫຼີກເວັ້ນການຫຍໍ້ມາຈາກເຫຼົ່ານີ້.UCOM, PCDHGB7, ແຍກແຍະຢ່າງມີປະສິດຕິພາບລະດັບສູງ lesions squamous intraepithelial (HSILs) ແລະມະເຮັງປາກມົດລູກຈາກຕົວຢ່າງປົກກະຕິ ແລະ lesions intraepithelial squamous ລະດັບຕ່ໍາ (LSILs), ໃນຂະນະທີ່ເຄື່ອງຫມາຍຊີວະພາບອື່ນໆສ່ວນໃຫຍ່ສາມາດຈໍາແນກມະເຮັງປາກມົດລູກຈາກຕົວຢ່າງປົກກະຕິ30.ເຖິງແມ່ນວ່າ PCDHGB7 ບໍ່ໄດ້ກວດພົບຄວາມແຕກຕ່າງທີ່ສໍາຄັນລະຫວ່າງ endometrium ປົກກະຕິແລະ hyperplasia endometrial, ຄວາມແຕກຕ່າງທີ່ສໍາຄັນແມ່ນກວດພົບລະຫວ່າງ endometrium ປົກກະຕິແລະ hyperplasia atypical, ແລະຄວາມແຕກຕ່າງທີ່ໃຫຍ່ກວ່າແມ່ນກວດພົບລະຫວ່າງ endometrium ປົກກະຕິແລະມະເຮັງ endometrial (EC) ໂດຍອີງໃສ່ PCDHGB731.UCOMs ແມ່ນເປັນເອກະລັກຂອງ lesions malignant ໃນຖານຂໍ້ມູນແລະຕົວຢ່າງທາງດ້ານການຊ່ວຍ.ຈາກທັດສະນະຂອງຄົນເຈັບ, UCOMs ທີ່ບໍ່ຊ້ໍາກັນຫຼຸດລົງຂອບເຂດສໍາລັບການເຂົ້າໃຈຕົວຊີ້ບອກທີ່ຊັບຊ້ອນຂອງຕົວຊີ້ບອກ biomarkers ທີ່ບໍ່ຫມັ້ນຄົງທີ່ປະຕິບັດບໍ່ດີແລະຄວາມກັງວົນທີ່ສອດຄ້ອງກັນໃນລະຫວ່າງຂະບວນການປະເມີນຜົນ.ຈາກທັດສະນະຂອງຄລີນິກ, UCOMs ທີ່ມີເອກະລັກສະເພາະຄວາມແຕກຕ່າງຂອງມະເຮັງຈາກ lesions benign, ເຊິ່ງຊ່ວຍໃນ triage ຂອງຄົນເຈັບແລະຫຼຸດຜ່ອນຂັ້ນຕອນທາງການແພດທີ່ບໍ່ຈໍາເປັນແລະການປິ່ນປົວເກີນ.ດັ່ງນັ້ນ, UCOMs ທີ່ມີເອກະລັກສະເພາະຊ່ວຍຫຼຸດຜ່ອນການຊໍ້າຊ້ອນຂອງລະບົບການແພດ, ບັນເທົາຄວາມຫຍຸ້ງຍາກໃນລະບົບ, ແລະສ້າງຊັບພະຍາກອນທາງການແພດເພີ່ມເຕີມໃຫ້ແກ່ຜູ້ທີ່ຕ້ອງການ.
ຮູບທີ 1 ຕາຕະລາງການເຮັດວຽກຂອງ GPS ສໍາລັບການກວດຫາ DNA methylation25.ເສັ້ນສີຂີ້ເຖົ່າ: ປ້ອນລໍາດັບ DNA;ເສັ້ນສີແດງ: DNA ທີ່ໄດ້ຮັບການປິ່ນປົວດ້ວຍ T4 DNA polymerase, ທົດແທນ cytosine ດ້ວຍ 5′-methylcytosine ຢູ່ປາຍ 3′ ຂອງວັດສະດຸປ້ອນ;ສີຟ້າ C ກັບຂ້ອຍ: methylated cytosine;ສີຟ້າ C: unmethylated cytosine;ສີເຫຼືອງ T: thymine25.
ທັງຫມົດຫຼືບໍ່ມີຫຍັງ
UCOMs ມີຢູ່ໃນຈຸລັງມະເຮັງເທົ່ານັ້ນ ແລະຖືກກວດພົບຢ່າງໝັ້ນທ່ຽງໃນເກືອບທຸກຈຸລັງມະເຮັງ.HIST1H4F ໄດ້ຖືກກວດສອບວ່າເປັນ hypermethylated ໃນເກືອບທຸກປະເພດຂອງເນື້ອງອກແຕ່ບໍ່ແມ່ນຢູ່ໃນຕົວຢ່າງປົກກະຕິ27.ເຊັ່ນດຽວກັນ, PCDHGB7 ແລະ SIX6 ຍັງໄດ້ສະແດງໃຫ້ເຫັນວ່າມີ hypermethylated ໃນຕົວຢ່າງ tumor ທັງຫມົດແຕ່ບໍ່ແມ່ນຢູ່ໃນຕົວຢ່າງປົກກະຕິ 30-32.ລັກສະນະທີ່ເປັນເອກະລັກນີ້ປັບປຸງປະສິດທິພາບຂອງ UCOMs ຢ່າງຫຼວງຫຼາຍກ່ຽວກັບຂອບເຂດຈໍາກັດຂອງການກວດສອບແລະຄວາມອ່ອນໄຫວ.ມີພຽງແຕ່ 2% ຂອງຈຸລັງມະເຮັງສາມາດຖືກແຍກອອກໄດ້ໃນຕົວຢ່າງ, ເຮັດໃຫ້ UCOMs ເປັນ biomarker ທີ່ມີຄວາມອ່ອນໄຫວຫຼາຍກ່ວາ biomarkers ທີ່ມີຢູ່ຫຼາຍທີ່ສຸດ 30. ໃນຖານະເປັນ biomarker ທີ່ໃຊ້ໃນການກວດຫາມະເຮັງ colorectal, ການກາຍພັນຂອງ KRAS ມີພຽງແຕ່ປະມານ 36% ຂອງກໍລະນີມະເຮັງ colorectal, ສະເໜີຄວາມເປັນໄປໄດ້ໃນການວິນິດໄສທີ່ບໍ່ດີ33.ອັດຕາສ່ວນຕໍ່າຂອງການກາຍພັນຂອງ KRAS ໃນມະເຮັງກະເພາະລໍາໃສ້ຈໍາກັດ KRAS ໃນການປະສົມປະສານກັບ biomarkers ອື່ນໆ.ໃນຄວາມເປັນຈິງ, ການປະສົມປະສານຂອງ biomarkers ອາດຈະເບິ່ງຄືວ່າມີແນວໂນ້ມໃນຕອນຕົ້ນ, ແຕ່ບໍ່ສະເຫມີໄປສ້າງຜົນໄດ້ຮັບທີ່ຫນ້າພໍໃຈໃນຂະນະທີ່ສະແດງໃຫ້ເຫັນສິ່ງລົບກວນຫຼາຍກວ່າເກົ່າໃນການວິເຄາະການຊອກຄົ້ນຫາແລະປົກກະຕິແລ້ວກ່ຽວຂ້ອງກັບຂັ້ນຕອນການທົດລອງທີ່ສັບສົນຫຼາຍ.ໃນທາງກົງກັນຂ້າມ, PCDHGB7 ແລະ UCOMs ອື່ນໆມີຢູ່ໃນມະເຮັງທັງຫມົດ.UCOMs ກວດພົບອົງປະກອບທີ່ເປັນມະເຮັງໃນຕົວຢ່າງມະເຮັງປະເພດຕ່າງໆດ້ວຍຄວາມແມ່ນຍໍາທີ່ສຸດໃນຂະນະທີ່ກໍາຈັດຂະບວນການວິເຄາະການຍົກເລີກສຽງທີ່ສັບສົນ.ມັນບໍ່ຍາກທີ່ຈະກວດພົບມະເຮັງໃນຕົວຢ່າງທີ່ອຸດົມສົມບູນ, ແຕ່ມັນເປັນສິ່ງທ້າທາຍທີ່ສຸດທີ່ຈະກວດພົບມະເຮັງໃນຕົວຢ່າງຂະຫນາດນ້ອຍ.UCOMs ມີຄວາມສາມາດກວດຫາມະເຮັງໃນປະລິມານໜ້ອຍ.
ຮູບທີ 2 ລັກສະນະຂອງ UCOMs.
ການກວດຫາມະເຮັງກ່ອນການປ່ຽນແປງທາງ pathological
UCOMs ສາມາດກວດພົບໄດ້ຢູ່ໃນຂັ້ນຕອນຂອງການເປັນມະເຮັງກ່ອນການປ່ຽນແປງທາງ pathological.ໃນຖານະເປັນ biomarkers epigenetic, ຄວາມຜິດປົກກະຕິ UCOM ເກີດຂື້ນໃນຂັ້ນຕອນກ່ອນຫນ້າກ່ວາຄວາມຜິດປົກກະຕິຂອງ phenotypic ແລະສາມາດກວດພົບໄດ້ຕະຫຼອດ tumorigenesis, ຄວາມກ້າວຫນ້າ, ແລະ metastasis34,35.ຄວາມອ່ອນໄຫວຂອງ UCOM ໃນໄລຍະເວລາຊ່ວຍເພີ່ມປະສິດທິພາບຂອງ UCOM ໃນການກວດຫາມະເຮັງໄລຍະຕົ້ນແລະບາດແຜກ່ອນມະເຮັງ.ການກວດຫາມະເຮັງຂັ້ນຕົ້ນໂດຍອີງໃສ່ການກວດ biopsies ແລະ cytology ອາດຈະເປັນເລື່ອງຍາກສໍາລັບແພດຫມໍທີ່ມີປະສົບການຫຼາຍທີ່ສຸດ.ການກວດ biopsy ດຽວທີ່ໄດ້ມາໂດຍຜ່ານ colposcopy ໄດ້ຖືກລາຍງານວ່າເປັນບວກໃນ 60.6% ຂອງຕົວຢ່າງ HSIL+.ຕ້ອງມີການກວດ biopsies ເພີ່ມເຕີມສໍາລັບ lesions ຫຼາຍເພື່ອເພີ່ມຄວາມອ່ອນໄຫວ36.ໃນທາງກົງກັນຂ້າມ, UCOM, PCDHGB7, ມີຄວາມອ່ອນໄຫວຂອງ 82% ສໍາລັບຕົວຢ່າງ HSIL+, ເກີນຄວາມອ່ອນໄຫວຂອງ biopsies ແລະ biomarkers30 ຫຼາຍທີ່ສຸດ.ເຄື່ອງໝາຍ methylation, FAM19A4, ມີຄວາມອ່ອນໄຫວ 69% ສໍາລັບ CIN2+, ເຊິ່ງຄ້າຍຄືກັບ cytology, ແຕ່ບໍ່ສາມາດແຍກ CIN1 ຈາກຕົວຢ່າງປົກກະຕິ37.UCOMs ໄດ້ຖືກສະແດງໃຫ້ເຫັນວ່າເປັນຕົວຊີ້ບອກ biomarker ເບື້ອງຕົ້ນທີ່ລະອຽດອ່ອນກວ່າ.ເມື່ອປຽບທຽບກັບຜູ້ຊ່ຽວຊານດ້ານພະຍາດທີ່ອີງໃສ່ປະສົບການ, UCOMs ມີຄວາມອ່ອນໄຫວໃນການກວດສອບດີກວ່າສໍາລັບມະເຮັງໄລຍະຕົ້ນ, ເຊິ່ງປະກອບສ່ວນເຂົ້າໃນການປັບປຸງການຄາດເດົາຂອງມະເຮັງແລະການຢູ່ລອດ30.ນອກຈາກນັ້ນ, UCOMs ສະເຫນີແພລະຕະຟອມການກວດພົບທີ່ສາມາດເຂົ້າເຖິງເຂດທີ່ຂາດແພດຫມໍທີ່ມີປະສົບການແລະປັບປຸງປະສິດທິພາບການກວດສອບຢ່າງຫຼວງຫຼາຍ.ດ້ວຍການເກັບຕົວຢ່າງ ແລະ ຂັ້ນຕອນການກວດຫາທີ່ເປັນເອກະພາບ, ການກວດຫາ UCOM ໃຫ້ຜົນໄດ້ຮັບທີ່ໝັ້ນຄົງ ແລະ ງ່າຍໃນການຕີຄວາມໝາຍທີ່ເໝາະສົມກັບພິທີການກວດກາທີ່ຕ້ອງການພະນັກງານ ແລະ ຊັບພະຍາກອນທາງການແພດໜ້ອຍກວ່າ.
ງ່າຍທີ່ຈະກວດພົບ
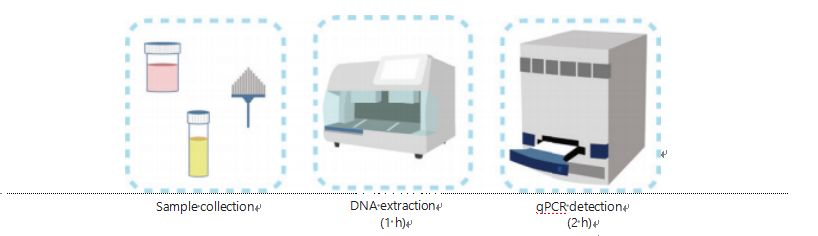
ວິທີການປະຈຸບັນໃນການກວດສອບ DNA methylation ແມ່ນສັບສົນແລະໃຊ້ເວລາຫຼາຍ.ວິທີການສ່ວນໃຫຍ່ຮຽກຮ້ອງໃຫ້ມີການຫັນເປັນ bisulfite, ເຊິ່ງເຮັດໃຫ້ການສູນເສຍຄຸນນະພາບຂອງຕົວຢ່າງແລະອາດຈະເຮັດໃຫ້ຜົນໄດ້ຮັບທີ່ບໍ່ຫມັ້ນຄົງແລະບໍ່ຖືກຕ້ອງ.ການສືບພັນທີ່ບໍ່ດີທີ່ເກີດຈາກການປິ່ນປົວ bisulfite ອາດຈະເຮັດໃຫ້ເກີດຄວາມສັບສົນຕໍ່ແພດແລະຄົນເຈັບແລະແຊກແຊງຕື່ມອີກກັບກົນລະຍຸດການຕິດຕາມແລະ / ຫຼືການປິ່ນປົວ.ດັ່ງນັ້ນ, ພວກເຮົາປັບປຸງວິທີການກວດຫາ UCOM ຕື່ມອີກເພື່ອຫຼີກລ່ຽງການປິ່ນປົວແບບ bisulfite ທີ່ເປັນບັນຫາຂອງຕົວຢ່າງ, ຮອງຮັບຄວາມຕ້ອງການທາງດ້ານຄລີນິກ ແລະ ປັບປຸງການເຂົ້າເຖິງ.ພວກເຮົາໄດ້ພັດທະນາວິທີການໃຫມ່ໂດຍໃຊ້ enzymes ການຈໍາກັດ methylation-sensitive ປະສົມປະສານກັບ PCR ປະລິມານ fluorescent ທີ່ແທ້ຈິງ (Me-qPCR) ເພື່ອ quan- ສະຖານະການ methylation ຂອງ UCOMs ພາຍໃນ 3 ຊົ່ວໂມງໂດຍໃຊ້ຂັ້ນຕອນການຈັດການງ່າຍ (ຮູບ 3).Me-qPCR ສາມາດບັນຈຸຕົວຢ່າງຫຼາຍປະເພດ, ເຊັ່ນ: ການເກັບຕົວຢ່າງທາງຄລີນິກຂອງນໍ້າຍ່ຽວໃນຮ່າງກາຍ ແລະຕົວຢ່າງນໍ້າຍ່ຽວທີ່ເກັບເອົາເອງ.ຕົວຢ່າງທາງຄລີນິກທີ່ເກັບກໍາສາມາດຖືກປຸງແຕ່ງ, ເກັບຮັກສາ, ແລະດໍາເນີນການກວດສອບໄດ້ຢ່າງງ່າຍດາຍໂດຍໃຊ້ການສະກັດເອົາ DNA ມາດຕະຖານແລະອັດຕະໂນມັດ.DNA ທີ່ຖືກສະກັດຈາກນັ້ນສາມາດຖືກນໍາໃຊ້ໂດຍກົງກັບເວທີ Me-qPCR ສໍາລັບປະຕິກິລິຍາຫນຶ່ງຫມໍ້ແລະຜົນໄດ້ຮັບປະລິມານຜົນຜະລິດ.ຫຼັງຈາກການວິເຄາະຜົນໄດ້ຮັບແບບງ່າຍໆໂດຍໃຊ້ແບບຈໍາລອງການວິນິດໄສທີ່ເຫມາະແລະຖືກຕ້ອງກັບປະເພດມະເຮັງສະເພາະ, ການກໍານົດສຸດທ້າຍຂອງຜົນການກວດສອບ UCOM ໄດ້ຖືກຕີຄວາມຫມາຍແລະນໍາສະເຫນີເປັນມູນຄ່າເຄິ່ງປະລິມານ.ແພລະຕະຟອມ Me-qPCR ປະຕິບັດໄດ້ດີກວ່າ bisulfite-pyrosequencing ແບບດັ້ງເດີມໃນການກວດສອບ UCOM ໃນຂະນະທີ່ປະຫຍັດການປ່ຽນ bisulfite 3 ຊົ່ວໂມງ, ອີງຕາມ EZ DNA Methylation-Gold kit protocol.ແພລະຕະຟອມການກວດຫາ methylation ທີ່ມີນະວັດກໍາເຮັດໃຫ້ການກວດສອບ UCOM ມີຄວາມຫມັ້ນຄົງ, ຖືກຕ້ອງກວ່າ, ແລະສາມາດເຂົ້າເຖິງໄດ້ຫຼາຍຂຶ້ນ30.
ຮູບທີ 3 ຂະບວນການກວດຫາ UCOMs.ປະເພດຕົວຢ່າງປະກອບມີ BALF ຕົວຢ່າງມືອາຊີບ, ແປງ Pap, ແລະ/ຫຼືປັດສະວະທີ່ເກັບເອົາເອງ.ຂະບວນການສະກັດເອົາ DNA ສາມາດຖືກຈັດໃສ່ກັບເຄື່ອງສະກັດອັດຕະໂນມັດ, ຜະລິດຕະພັນທີ່ສາມາດກວດພົບໄດ້ໂດຍກົງໂດຍ qPCR.
ຄໍາຮ້ອງສະຫມັກຂອງ UCOMs
ມະເຮັງປອດ
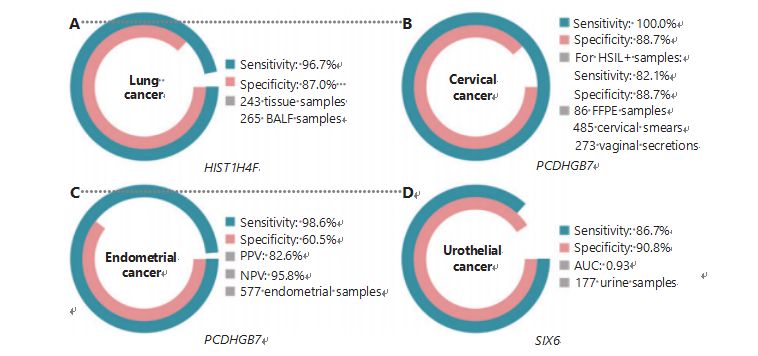
ມະເຮັງປອດແມ່ນເປັນມະເຮັງທີ່ກວດພົບເລື້ອຍໆເປັນອັນດັບສອງ ແລະເສຍຊີວິດຫຼາຍທີ່ສຸດໃນທົ່ວໂລກ, ກວມເອົາ 11.4% ຂອງກໍລະນີໃໝ່ ແລະ 18.0% ຂອງການເສຍຊີວິດໃໝ່1.ໃນບັນດາການວິນິດໄສທັງໝົດ, 85% ແມ່ນມະເຮັງປອດຂອງຈຸລັງຂະໜາດນ້ອຍ (NSCLC) ແລະ 15% ແມ່ນມະເຮັງປອດຈຸລັງຂະໜາດນ້ອຍ (SCLC), ເຊິ່ງມີລະດັບທີ່ສູງກວ່າຂອງ malignancy38.ການສະແກນ tomography ທີ່ໃຊ້ໃນປະລິມານຕໍ່າ (LDCT) ແມ່ນວິທີການກວດຫາມະເຮັງປອດທີ່ແນະນຳໃນປະຈຸບັນ ແລະ ໄດ້ຮັບການສະແດງເພື່ອປັບປຸງການກວດຫາໄວ ແລະ ຫຼຸດຜ່ອນອັດຕາການຕາຍ6;ແນວໃດກໍ່ຕາມ, ເນື່ອງຈາກຄວາມສະເພາະທີ່ຕໍ່າ ແລະການເຂົ້າເຖິງບໍ່ດີ, LDCT ຍັງບໍ່ທັນເປັນວິທີກວດທີ່ໜ້າພໍໃຈ, ຄືກັບເຄື່ອງໝາຍມະເຮັງທົ່ວໄປອື່ນໆ, ເຊັ່ນ CEA39.ຄ່າໃຊ້ຈ່າຍແລະທ່າແຮງສໍາລັບການວິນິດໄສທີ່ພາດແລະການວິນິດໄສທີ່ບໍ່ຖືກຕ້ອງຂອງຍຸດທະສາດການກວດ LDCT ຂັດຂວາງຄວາມກ້າວຫນ້າຂອງການໂຄສະນາການກວດຫາມະເຮັງປອດ40.HIST1H4F, UCOM, ມີທ່າແຮງອັນໃຫຍ່ຫຼວງເປັນຕົວຊີ້ບອກທາງຊີວະພາບໃນການກວດຫາຕົ້ນໆໃນຕົວຢ່າງຂອງນໍ້າ bronchoalveolar (BALF)27.HIST1H4F ແມ່ນ hypermethylated ໃນປອດ adenocar- cinoma ແລະມະເຮັງປອດ squamous cell carcinoma, ມີຄວາມສະເພາະຂອງການກວດຫາ 96.7% ແລະຄວາມອ່ອນໄຫວຂອງ 87.0% (ຮູບ 4A), ແລະປະສິດທິພາບພິເສດສໍາລັບມະເຮັງຂັ້ນຕອນ I27.HIST1H4F ມີຄວາມສະເພາະຂອງ 96.5% ແລະຄວາມອ່ອນໄຫວຂອງ 85.4% ສໍາລັບ NSCLC, ແລະ 96.5% ແລະ 95.7%, ຕາມລໍາດັບ, ສໍາລັບ SCLC27.ນອກຈາກນັ້ນ, ຕົວຢ່າງຂອງມະເຮັງອີກ 8 ຊະນິດ, ລວມທັງມະເຮັງຕ່ອມລູກໝາກ ແລະມະເຮັງລຳໄສ້ໃຫຍ່, ໄດ້ຢັ້ງຢືນວ່າ HIST1H4F ແມ່ນ hypermethylated ໃນທັງໝົດແປດຊະນິດ27.
ມະເຮັງປາກມົດລູກ
ມະເຮັງປາກມົດລູກເປັນມະເຮັງທີ່ກວດພົບເລື້ອຍໆເປັນອັນດັບທີ 4 ແລະເປັນສາເຫດອັນດັບທີ 4 ຂອງການເສຍຊີວິດຈາກມະເຮັງໃນແມ່ຍິງໃນປີ 2020, ເຊິ່ງກວມເອົາ 3.1% ຂອງກໍລະນີໃໝ່ ແລະ 3.4% ຂອງການເສຍຊີວິດຈາກມະເຮັງໃນທົ່ວໂລກ1.ເພື່ອກໍາຈັດມະເຮັງປາກມົດລູກໃນປີ 2030, ຕາມການສະເໜີຂອງອົງການອະນາໄມໂລກ, ການກວດຫາມະເຮັງປາກມົດລູກໄວແມ່ນມີຄວາມຈຳເປັນ.ຖ້າກວດພົບໃນໄລຍະເລີ່ມຕົ້ນ, ອັດຕາການຢູ່ລອດ 5 ປີເຖິງ 92% ດ້ວຍມະເຮັງປາກມົດລູກທີ່ແຜ່ລາມ41.ຄໍາແນະນໍາຂອງສະມາຄົມມະເຮັງອາເມລິກາ (ACS) ແນະນໍາການທົດສອບ cytology ປາກມົດລູກ, ການທົດສອບ HPV ເບື້ອງຕົ້ນ, ຫຼືການທົດສອບສໍາລັບການກວດສອບ42.Certology ປາກມົດລູກແມ່ນການບຸກລຸກແລະສາມາດກວດພົບພຽງແຕ່ 63.5% ຂອງກໍລະນີ CIN2+37.
PCDHGB7, ໃນທາງກົງກັນຂ້າມ, ໄດ້ປະຕິບັດໄດ້ດີກວ່າການໃຊ້ Pap smears ແລະຊ່ອງຄອດ, ແລະສາມາດແຍກແຍະ HSIL ຈາກ LSIL ໄດ້ຢ່າງມີປະສິດທິພາບໃນຂັ້ນຕອນຕົ້ນໆ.PCDHGB7 ດຽວມີຄວາມອ່ອນໄຫວ 100.0% ແລະຄວາມສະເພາະຂອງ 88.7% ສໍາລັບມະເຮັງປາກມົດລູກ (ຮູບ 4B), ແລະຄວາມອ່ອນໄຫວ 82.1% ແລະຄວາມຈໍາເພາະ 88.7% ສໍາລັບ HSIL+ ຕົວຢ່າງ30.PCDHGB7 ຍັງມີຄວາມອ່ອນໄຫວ 90.9% ແລະຄວາມສະເພາະຂອງ 90.4% ໃນຕົວຢ່າງຄວາມລັບຂອງຊ່ອງຄອດສໍາລັບມະເຮັງປາກມົດລູກ, ເຊິ່ງງ່າຍກວ່າຫຼາຍທີ່ຈະເກັບກໍາ30.ເມື່ອລວມກັບການທົດສອບຄວາມສ່ຽງສູງ (hr) HPV ຫຼື Thinprep Cytology Test (TCT), PCDHGB7 ມີຄວາມອ່ອນໄຫວເພີ່ມຂຶ້ນ 95.7% ແລະຄວາມສະເພາະຂອງ 96.2%, ຫຼາຍກວ່າການທົດສອບ hrHPV (20.3%), TCT (51.2% ຢ່າງຫຼວງຫຼາຍ. ), ແລະທັງສອງລວມກັນ (57.8%) ສໍາລັບມະເຮັງປາກມົດລູກ30.PCDHGB7 ຍັງໄດ້ຮັບການສະແດງໃຫ້ເຫັນວ່າເປັນ hypermethylated ໃນ 17 ປະເພດຂອງມະເຮັງຈາກຖານຂໍ້ມູນ TCGA, ຊີ້ໃຫ້ເຫັນເຖິງຄວາມເຫມາະສົມໃນ UCOM family30.
ຮູບທີ່ 4 UCOMs ໄດ້ຮັບການຢັ້ງຢືນຢູ່ໃນສີ່ປະເພດຂອງມະເຮັງໃນການສຶກສາທາງດ້ານຄລີນິກຂະຫນາດໃຫຍ່.A. ປະສິດທິພາບຂອງ HIST1H4F, UCOM, ໃນການກວດຫາມະເຮັງປອດຂອງ 508 ຕົວຢ່າງ.B. ການປະຕິບັດຂອງ PCDHGB7, UCOM, ໃນການກວດຫາມະເຮັງປາກມົດລູກຂອງ 844 ຕົວຢ່າງ.C. ປະສິດທິພາບຂອງ PCDHGB7, UCOM, ໃນການກວດຫາມະເຮັງ endometrial ຂອງ 577 endometrial Pap ແລະ Tao ແປງຕົວຢ່າງ.D. ການປະຕິບັດຂອງ SIX6, UCOM, ໃນການກວດຫາມະເຮັງ urothelial ຂອງ 177 ຕົວຢ່າງ.
EC
EC ເປັນມະເຮັງລະບົບຈະເລີນພັນຂອງເພດຍິງທີ່ພົບເລື້ອຍທີ່ສຸດໃນທົ່ວໂລກ, ມີຜູ້ຕິດເຊື້ອໃໝ່ປະມານ 4.2 ລ້ານຄົນ ແລະ 1% ຂອງການເສຍຊີວິດຍ້ອນມະເຮັງຕໍ່ປີ1.ດ້ວຍການວິນິດໄສທີ່ປະສົບຜົນ ສຳ ເລັດຢູ່ໃນຂັ້ນຕອນ anearly, EC ສາມາດປິ່ນປົວໄດ້ແລະມີອັດຕາການຢູ່ລອດ 5 ປີຂອງ 95% ສໍາລັບມະເຮັງຂັ້ນຕອນ I.ຄົນເຈັບທີ່ມີອາການ, ເຊັ່ນ: ເລືອດອອກຂອງມົດລູກຜິດປົກກະຕິ, ໄດ້ຮັບການປະເມີນຜົນທາງດ້ານຄລີນິກເປັນໄລຍະແລະຜ່ານຂັ້ນຕອນການກວດຫາເຊື້ອທີ່ຮຸກຮານແລະເຈັບປວດ, ເຖິງວ່າຈະມີພຽງແຕ່ 5% ຫາ 10% ໃນທີ່ສຸດກໍ່ຈະພັດທະນາ EC43.transvaginal ultra-sound, ເປັນວິທີການກວດຫາທົ່ວໄປ, ແມ່ນບໍ່ມີຄວາມຫນ້າເຊື່ອຖືສູງເນື່ອງຈາກຄວາມບໍ່ສາມາດທີ່ຈະແຍກຄວາມແຕກຕ່າງຂອງ benign ຈາກການປ່ຽນແປງ endo-metrial malignant ແລະອັດຕາບວກສູງທີ່ບໍ່ຖືກຕ້ອງ 44.
ການປຽບທຽບຂະຫນານຂອງ serum CA-125, ເຄື່ອງຫມາຍ biomarker EC ທີ່ຖືກປະຕິບັດຢ່າງກວ້າງຂວາງ, ແລະ PCDHGB7 ໄດ້ດໍາເນີນການ.Serum CA-125 ມີຄວາມອ່ອນໄຫວຂອງ 24.8%, ເຊິ່ງຊີ້ໃຫ້ເຫັນວ່າ CA-125 ເປັນເຄື່ອງຫມາຍທີ່ບໍ່ພຽງພໍສໍາລັບ EC ເຖິງວ່າຈະມີຄວາມສະເພາະຂອງ 92.3% 31.ການກວດຫາ PCDHGB7 ໂດຍໃຊ້ຕົວຢ່າງຂອງແປງ Pap ໃຫ້ຄວາມອ່ອນໄຫວຂອງ 80.65% ແລະຄວາມສະເພາະຂອງ 82.81% ສໍາລັບຂັ້ນຕອນ ECatall, ໃນຂະນະທີ່ແປງ Tao ມີຄວາມອ່ອນໄຫວ 61.29% ແລະຄວາມສະເພາະຂອງ 95.31% 31.ຮູບແບບການວິນິດໄສ PCDHGB7, ໂດຍອີງໃສ່ Me-qPCR, ໃຫ້ຄວາມອ່ອນໄຫວຂອງ 98.61%, ສະເພາະຂອງ 60.5%, ແລະຄວາມຖືກຕ້ອງໂດຍລວມຂອງ 85.5%, ໂດຍໃຊ້ຕົວຢ່າງ Pap ແລະ Tao brush (ຮູບ 4C)31.
ມະເຮັງ urothelial
ມະເຮັງ urothelial, ປະກອບດ້ວຍພົກຍ່ຽວ, pelvis renal, ແລະມະເຮັງທໍ່ຍ່ຽວ, ເປັນມະເຮັງທີ 7 ທີ່ຖືກກວດພົບເລື້ອຍໆທີ່ສຸດໃນປີ 2020 ໃນທົ່ວໂລກ, ເຊິ່ງກໍ່ໃຫ້ເກີດກໍລະນີໃຫມ່ 5.2% ແລະ 3.9% ຂອງການເສຍຊີວິດ1.ມະເຮັງ urothelial, ຫຼາຍກວ່າ 50% ທີ່ເປັນມະເຮັງພົກຍ່ຽວ, ເປັນມະເຮັງທີ່ກວດພົບເລື້ອຍໆອັນດັບທີ 4 ໃນສະຫະລັດໃນປີ 2022, ເຊິ່ງກວມເອົາ 11.6% ຂອງກໍລະນີທີ່ກວດພົບໃໝ່3.ປະມານ 75% ຂອງມະເຮັງພົກຍ່ຽວຖືກຈັດປະເພດເປັນມະເຮັງພົກຍ່ຽວທີ່ບໍ່ແມ່ນກ້າມ ທີ່ຖືກຈຳກັດຢູ່ໃນເຍື່ອເມືອກ ຫຼື submucosa45.A cystoscopy biopsy ແມ່ນມາດຕະຖານຄໍາສໍາລັບການວິນິດໄສມະເຮັງ urothelial ປະຕິບັດໂດຍ fluorescence ໃນ situ hybridization (FISH) ແລະການທົດສອບ cytology.FISH ແລະ cytology ມີປະສິດທິພາບການວິນິດໄສທີ່ບໍ່ດີ, ແລະ cystoscopy ເປັນການລົບກວນແລະມີຄວາມສ່ຽງພື້ນຖານຂອງ microlesions ທີ່ຂາດຫາຍໄປ, ການແປຄວາມຫມາຍທີ່ບໍ່ຖືກຕ້ອງ, ແລະອາດຈະເຮັດໃຫ້ເກີດການແຜ່ກະຈາຍຫຼືການເກີດຂອງມະເຮັງ46.UCOM ທີ່ຖືກຕ້ອງກ່ອນຫນ້ານີ້, PCDHGB7, ຍັງໄດ້ຖືກສະແດງໃຫ້ເຫັນວ່າມີ hypermethylated ໃນມະເຮັງ urothelial, ທີ່ມີພື້ນທີ່ພາຍໃຕ້ເສັ້ນໂຄ້ງຂອງ 0.86, ຊີ້ໃຫ້ເຫັນເຖິງຄວາມສາມາດໃນການວິນິດໄສທີ່ເປັນໄປໄດ້30.ເພື່ອກວດສອບ UCOMs ເພີ່ມເຕີມແລະຮອງຮັບປະເພດຕົວຢ່າງທີ່ດີກວ່າ, SIX6, UCOM ນິຍາຍ, ໄດ້ຖືກກວດສອບແລະສະແດງໃຫ້ເຫັນທ່າແຮງການວິນິດໄສທີ່ດີເລີດໃນການກວດພົບມະເຮັງ urothelial ໃນຕົ້ນໆໂດຍໃຊ້ຕົວຢ່າງນໍ້າຍ່ຽວໃນເວທີ Me-qPCR.ການກວດຫາ SIX6 ໂດຍໃຊ້ຕົວຢ່າງປັດສະວະສະແດງໃຫ້ເຫັນເຖິງຄວາມອ່ອນໄຫວໃນການແຂ່ງຂັນຂອງ 86.7% ແລະຄວາມສະເພາະຂອງ 90.8% (ຮູບ 4D), ໃນຂະນະທີ່ບໍ່ແມ່ນການບຸກລຸກແລະງ່າຍທີ່ຈະໄດ້ຮັບ32.ທ່າແຮງຂອງ SIX6 ໃນການຕິດຕາມກວດກາ metastasis ແລະການປະເມີນຜົນປະສິດທິພາບການປິ່ນປົວແມ່ນຢູ່ພາຍໃຕ້ການສືບສວນ.
ອະນາຄົດ ແລະສິ່ງທ້າທາຍ
UCOMs ມີການປະຕິບັດທີ່ເຂັ້ມແຂງໃນທ່າແຮງການວິນິດໄສຂອງມະເຮັງຫຼາຍຊະນິດ, ແຕ່ຍັງມີວຽກຫຼາຍທີ່ຕ້ອງເຮັດ.ພວກເຮົາໄດ້ຂະຫຍາຍບັນຊີລາຍຊື່ຂອງ UCOM ແລະໄດ້ດໍາເນີນການກວດສອບ UCOMs ຢ່າງຈິງຈັງໃນປະເພດມະເຮັງຫຼາຍຂຶ້ນ, ລວມທັງສິ່ງທີ່ເປັນປະເພນີທີ່ຍາກທີ່ຈະກວດພົບ.ຜົນໄດ້ຮັບການກວດສອບຈາກຖານຂໍ້ມູນ TCGA ໄດ້ຢືນຢັນການສະຫມັກຂອງ UCOM ໃນຫຼາຍປະເພດຂອງມະເຮັງແລະສະຖານະການອື່ນໆ.ໃນການສືບສວນເບື້ອງຕົ້ນ, UCOMs ໄດ້ຖືກສະແດງໃຫ້ເຫັນວ່າມີທ່າແຮງການວິນິດໄສທີ່ເຂັ້ມແຂງສໍາລັບ cholangiocarcinomas ແລະ adenocarcinomas pancreatic, ເຊິ່ງເກືອບເປັນໄປບໍ່ໄດ້ທີ່ຈະວິນິດໄສໃນຂັ້ນຕອນ anearly ດ້ວຍວິທີການກວດສອບໃນປະຈຸບັນ32,47.ຄວາມສາມາດໃນການກວດພົບມະເຮັງທີ່ຫາຍາກດ້ວຍ UCOMs ສາມາດນໍາໃຊ້ກັບ DNA tumor circulating (ctDNA) ໂດຍການປັບປຸງ biopsy platform48.ການສຶກສາທີ່ກ່ຽວຂ້ອງກັບຄະນະກວດຫາມະເຮັງ DNA ທີ່ອີງໃສ່ plasma plasma ໄດ້ໃຫ້ຜົນຄວາມອ່ອນໄຫວ 57.9% 49.ເຖິງວ່າຈະມີຄວາມສະເພາະສູງ, ການປະຕິບັດໂດຍລວມສະແດງໃຫ້ເຫັນວ່າຍັງມີຫ້ອງສໍາລັບການປັບປຸງ.
ຄຸນລັກສະນະທີ່ເປັນເອກະລັກຂອງ UCOMs ຍັງໄດ້ສະຫນັບສະຫນູນການສືບສວນກ່ຽວກັບທ່າແຮງຂອງ UCOM ໃນການປະເມີນປະສິດທິພາບການປິ່ນປົວແລະການຕິດຕາມການເກີດໃຫມ່.ອີງຕາມເງື່ອນໄຂການປະເມີນຜົນການຕອບສະຫນອງໃນເນື້ອງອກແຂງ (RECIST), ການຖ່າຍຮູບທາງການແພດແມ່ນວິທີການແນະນໍາສໍາລັບການຕິດຕາມການເກີດໃຫມ່ແລະການປະເມີນປະສິດທິພາບການປິ່ນປົວ, ໃນຂະນະທີ່ເຄື່ອງຫມາຍ tumor ຖືກນໍາໃຊ້ຢ່າງດຽວສໍາລັບການປະເມີນ 50.ໃນຄວາມເປັນຈິງ, ແນວໃດກໍ່ຕາມ, ວິທີການຮູບພາບໄດ້ຮັບຜົນກະທົບຢ່າງຫຼວງຫຼາຍໂດຍຄວາມຖີ່ແລະເວລາ, ແລະດັ່ງນັ້ນຈິ່ງເຮັດໃຫ້ຄົນເຈັບມີຄວາມສ່ຽງສູງແລະຄ່າໃຊ້ຈ່າຍ 51,52.SIX6 ໄດ້ຮັບການກວດສອບເພື່ອເປັນຕົວຊີ້ວັດການແຜ່ກະຈາຍຂອງມະເຮັງເຕົ້ານົມ 32.ການກວດສອບ ctDNA ທີ່ອີງໃສ່ການກວດຮ່າງກາຍຂອງແຫຼວເຮັດໃຫ້ການເຝົ້າລະວັງແບບສົດໆໃນໄລຍະເດືອນຂອງພະຍາດທີ່ຕົກຄ້າງໜ້ອຍທີ່ສຸດກ່ອນການກວດຫາທາງລັງສີ, ເໝາະແກ່ການຊັກຊ້າ ແລະປ້ອງກັນການແຜ່ລະບາດຂອງມະເຮັງທີ່ກ່ຽວຂ້ອງກັບການເກີດຄືນໃຫມ່53.ຜົນໄດ້ຮັບເບື້ອງຕົ້ນຊີ້ໃຫ້ເຫັນວ່າ UCOMs ສະທ້ອນໃຫ້ເຫັນເຖິງລະດັບຂອງ hypermethylation ມະເຮັງໃນເວລາທີ່ແທ້ຈິງທັນທີຫຼັງຈາກການຜ່າຕັດແລະການປິ່ນປົວ32.ຄວາມອ່ອນໄຫວສູງທີ່ສະແດງໂດຍ UCOMs ແລະການນໍາໄປໃຊ້ໃນຫຼາຍໆຊະນິດທີ່ບໍ່ມີການລົບກວນເຮັດໃຫ້ UCOMs ສາມາດຮັບໃຊ້ເປັນ biomarker mon-itoring ທີ່ຊັດເຈນໃນຂະນະທີ່ຮັກສາການປະຕິບັດຕາມຄົນເຈັບສູງ.
ໃນເວລາດຽວກັນ, ການເຂົ້າເຖິງສາທາລະນະໃນການທົດສອບແມ່ນອີກບັນຫາໃຫຍ່ທີ່ຮຽກຮ້ອງໃຫ້ມີຄວາມພະຍາຍາມເພີ່ມເຕີມ.ໃນຂະນະທີ່ການຮ່ວມມືການຊອກຄົ້ນຫາ UCOM ໄດ້ຖືກຮັບຮອງເອົາຢູ່ໃນໂຮງຫມໍຫຼາຍຂື້ນໃນຄວາມຫວັງທີ່ຈະໃຫ້ຜົນປະໂຫຍດແກ່ຄົນເຈັບຫຼາຍຂຶ້ນ, ການກວດຫາແລະການກວດຫາແບບມືອາຊີບໄດ້ຖືກປະຕິບັດຢ່າງຫ້າວຫັນໃນຊົນນະບົດຂອງຈີນ.UCOMs ຕ້ອງການການປັບປຸງການເຂົ້າເຖິງເພື່ອໃຫ້ມີຄຸນສົມບັດເປັນເຄື່ອງມືກວດສອບທີ່ເປັນໄປໄດ້, ໂດຍສະເພາະສໍາລັບພື້ນທີ່ດ້ອຍພັດທະນາ.
ໃນຂະນະທີ່ຜົນຂອງຄໍາຮ້ອງສະຫມັກ UCOM ໃນການກວດພົບເບື້ອງຕົ້ນແມ່ນມີຄວາມມຸ່ງຫວັງ, ມີຫຼາຍສິ່ງທີ່ບໍ່ຮູ້ກ່ຽວກັບ UCOM.ດ້ວຍການສໍາຫຼວດຢ່າງຫ້າວຫັນ, ການຄົ້ນຄວ້າເພີ່ມເຕີມແມ່ນຮັບປະກັນວ່າເປັນຫຍັງ UCOMs ແມ່ນມີຢູ່ໃນໂລກມະເຮັງ.ກົນໄກກົດລະບຽບການສືບພັນທາງພັນທຸກໍາທີ່ຕິດພັນກັບ UCOMs ແມ່ນສົມຄວນທີ່ຈະສືບສວນຕື່ມອີກ, ເຊິ່ງສາມາດຊີ້ໃຫ້ເຫັນທິດທາງໃຫມ່ສໍາລັບການປິ່ນປົວມະເຮັງ.ກັບຄືນສູ່ການພົວພັນລະຫວ່າງຄວາມຄ້າຍຄືກັນຂອງເນື້ອງອກແລະ heterogeneity, ພວກເຮົາສົນໃຈວ່າເປັນຫຍັງ UCOMs ສາມາດເປັນຂໍ້ຍົກເວັ້ນຂອງຕົວຊີ້ບອກຂອງມະເຮັງສ່ວນໃຫຍ່ທີ່ຕິດພັນກັບປະເພດມະເຮັງສະເພາະ.ບົດບາດຂອງຄວາມຜິດປົກກະຕິຂອງ DNA methylation ຂອງ UCOM ໃນ tumorigenesis, ຄວາມຄືບຫນ້າຂອງເນື້ອງອກ, ແລະ metastasis ບໍ່ໄດ້ຖືກ ກຳ ນົດໃນຂະບວນການສູນເສຍແລະຟື້ນຟູຕົວຕົນຂອງເຊນແລະ ຈຳ ເປັນຕ້ອງມີການກວດສອບຢ່າງລະອຽດ.ຄວາມສົນໃຈທີ່ສໍາຄັນອີກອັນຫນຶ່ງແມ່ນຢູ່ໃນຂອບເຂດຂອງການລວມເອົາລັກສະນະດຽວກັນຂອງ UCOMs ກັບເຄື່ອງຫມາຍທີ່ເປັນເອກະລັກຂອງເນື້ອເຍື່ອໃນຄວາມຫວັງທີ່ຈະເຂົ້າຫາການກວດພົບທີ່ຊັດເຈນຂອງຮ່ອງຮອຍຂອງມະເຮັງແລະການກໍານົດຕົ້ນກໍາເນີດຂອງເນື້ອເຍື່ອໃນລັກສະນະປີ້ນກັບກັນ.UCOMs ສາມາດເປັນເຄື່ອງມືທີ່ເຫມາະສົມເພື່ອປ້ອງກັນມະເຮັງ, ກວດຫາມະເຮັງ, ແລະມີທ່າແຮງປ້ອງກັນແລະລົບລ້າງມະເຮັງ.
ໃຫ້ການສະໜັບສະໜູນ
ວຽກງານນີ້ໄດ້ຮັບການສະຫນັບສະຫນູນຈາກໂຄງການ R&D ຫຼັກແຫ່ງຊາດຂອງຈີນ (ການຊ່ວຍເຫຼືອລ້າ No. 2022BEG01003), ມູນນິທິວິທະຍາສາດທໍາມະຊາດແຫ່ງຊາດຂອງຈີນ (ການຊ່ວຍເຫຼືອລ້າ No. , ແລະທຶນຊ່ວຍເຫຼືອລ້າຈາກສະຖາບັນວິທະຍາສາດ ແລະເຕັກໂນໂລຊີ Heze (Grant No. 2021KJPT07).
ຖະແຫຼງການຂັດແຍ້ງດ້ານຜົນປະໂຫຍດ
Wei Li ເປັນຜູ້ອໍານວຍການ R&D ຂອງບໍລິສັດ Shanghai Epiprobe Biotechnology Co., Ltd. Wenqiang Yu ຮັບໃຊ້ໃນຄະນະທີ່ປຶກສາວິທະຍາສາດຂອງ Epiprobe.W. Yu ແລະ Epiprobe ໄດ້ອະນຸມັດສິດທິບັດທີ່ຍັງຄ້າງທີ່ກ່ຽວຂ້ອງກັບວຽກງານນີ້.ຜູ້ຂຽນອື່ນໆທັງຫມົດປະກາດວ່າບໍ່ມີຜົນປະໂຫຍດແຂ່ງຂັນ.
ການປະກອບສ່ວນຂອງຜູ້ຂຽນ
Conceived ແລະອອກແບບໂຄງການ: Chengchen Qian ແລະ Wenqiang Yu.
ຂຽນເອກະສານ: Chengchen Qian.
ສ້າງຮູບພາບ: Chengchen Qian.
ການທົບທວນຄືນແລະດັດແກ້ຫນັງສືໃບລານ: Xiaolong Zou, Wei Li, Yinshan Li ແລະ Wenqiang Yu.
ເອກະສານອ້າງອີງ
1. Sung H, Ferlay J, Siegel RL, LaversanneM, Soerjomataram I, Jemal A, et al.ສະຖິຕິໂລກມະເຮັງ 2020: ການຄາດຄະເນຂອງ GLOBOCAN ຂອງ
ອັດຕາການຕາຍຂອງໂລກເປັນມະເຮັງ 36 ຄົນໃນ 185 ປະເທດ.CA Cancer J Clin.2021;71:209-49.
2. Xia C, Dong X, Li H, Cao M, Sun D, He S, et al.ສະຖິຕິມະເຮັງໃນຈີນແລະສະຫະລັດອາເມລິກາ, 2022: ຂໍ້ມູນ, ແນວໂນ້ມ, ແລະຕົວກໍານົດ.Chin MedJ (ພາສາອັງກິດ).2022;135:584-90.
3. Siegel RL, Miller KD, WagleNS, JemalA.ສະຖິຕິມະເຮັງ, 2023. CA Cancer J Clin.2023;73:17-48 .
4. Crosby D, BhatiaS, Brindle KM, Coussens LM, Dive C, Emberton M, et al.ການກວດພົບມະເຮັງໄວ.ວິທະຍາສາດ.2022;375: eaay9040.
5. Ladabaum U, Dominitz JA, KahiC, Schoen RE.ຍຸດທະສາດສໍາລັບ
ການກວດຫາມະເຮັງລຳໄສ້ໃຫຍ່.ກະເພາະອາຫານ.2020;158:418-32 .
6. Tanoue LT, Tanner NT, Gould MK, Silvestri GA.ການກວດຫາມະເຮັງປອດ.Am J Respir Crit Care Med.ປີ 2015;191:19-33.
7. Bouvard V, WentzensenN, Mackie A, Berkhof J, BrothertonJ, Giorgi-Rossi P, et al.ທັດສະນະຂອງ IARC ກ່ຽວກັບການກວດມະເຮັງປາກມົດລູກ.N EnglJ Med.2021;385: 1908-18.
8. Xue P, Ng MTA, QiaoY.ສິ່ງທ້າທາຍຂອງ colposcopy ສໍາລັບການກວດມະເຮັງປາກມົດລູກໃນ LMICs ແລະວິທີແກ້ໄຂໂດຍປັນຍາປະດິດ.BMC Med.2020;໑໘:໑໖໙ .
9. Johnson P, Zhou Q, Dao DY, Lo YMD.ໝູນວຽນເຄື່ອງໝາຍຊີວະພາບໃນການວິນິດໄສ ແລະ ຄຸ້ມຄອງມະເຮັງຕັບ.Nat Rev Gastroenterol Hepatol.2022;19:670-81.
10. Van PoppelH, Albreht T, Basu P, HogenhoutR, CollenS, Roobol M. Serum PSA-based ການກວດຫາມະເຮັງຕ່ອມລູກໝາກໃນເອີຣົບ ແລະທົ່ວໂລກ: ໃນອະດີດ, ປັດຈຸບັນ ແລະອະນາຄົດ.Nat Rev Urol.2022;19:
562-72.
11. HolyoakeA, O'Sullivan P, Pollock R, Best T, Watanabe J, KajitaY,
et al.ການພັດທະນາການກວດປັດສະວະແບບ multiplex RNA ສໍາລັບການກວດຫາແລະການແບ່ງຊັ້ນຂອງ carcinoma ເຊນຂ້າມຜ່ານຂອງພົກຍ່ຽວ.Clin Cancer Res.2008;14:742-9.
12. Feinberg AP, Vogelstein B. Hypomethylation distinguishes genes ຂອງມະເຮັງຂອງມະນຸດບາງຈາກຄູ່ຮ່ວມງານປົກກະຕິຂອງເຂົາເຈົ້າ.ທໍາມະຊາດ.ປີ 1983;301:89-92.
13. Ng JM, Yu J. ສົ່ງເສີມ hypermethylation ຂອງ genes suppressor tumor ເປັນ biomarkers ທ່າແຮງໃນມະເຮັງລໍາໄສ້ໃຫຍ່.IntJ Mol Sci.ປີ 2015;16:2472-96.
14. Esteller M. ມະເລັງ epigenomics: DNA methylomes ແລະແຜນທີ່ການດັດແກ້ histone.Nat Rev Genet.2007;8:286-98.
15. Nishiyama A, Nakanishi M. ການນໍາທາງພູມສັນຖານ DNA methylation ຂອງມະເຮັງ.ແນວໂນ້ມ Genet.2021;37:1012-27 .
16. Xie W, Schultz MD, ListerR, Hou Z, Rajagopal N, Ray P, et al.ການວິເຄາະ Epigenomic ຂອງຄວາມແຕກຕ່າງຫຼາຍເສັ້ນຂອງຈຸລັງລໍາຕົ້ນຂອງ embryonic ຂອງມະນຸດ.ເຊລ.ປີ 2013;153:1134-48.
17. Li Y, Zheng H, Wang Q, Zhou C, WeiL, Liu X, et al.ການວິເຄາະທົ່ວ Genome ເປີດເຜີຍບົດບາດຂອງ Polycomb ໃນການສົ່ງເສີມການ hypomethylation ຂອງ DNA methylation valleys.ພັນທຸ ກຳ ຊີວະພາບ.ປີ 2018;19:18 .
18. Koch A, JoostenSC, Feng Z, de Ruijter TC, DrahtMX, MelotteV,
et al.ການວິເຄາະ DNA methylation ໃນມະເຮັງ: ສະຖານທີ່ revisited.Nat Rev Clin Oncol.ປີ 2018;15:459-66.
19. KleinEA, Richards D, Cohn A, TummalM, Lapham R, Cosgrove D, et al.ການກວດສອບທາງຄລີນິກຂອງການທົດສອບການກວດຫາໂຣກມະເຮັງຫຼາຍຕົ້ນທີ່ອີງໃສ່ methylation ເປົ້າໝາຍໂດຍໃຊ້ຊຸດການກວດສອບເອກະລາດ.Ann Oncol.2021;32:1167-77.
20. Hanahan D, Weinberg RA.ຈຸດເດັ່ນຂອງມະເຮັງ.ເຊລ.2000;100:57-70.
21. Hanahan D. ຈຸດເດັ່ນຂອງມະເຮັງ: ຂະຫນາດໃຫມ່.ມະເຮັງ Discov.2022;12:31-46 .
22. Schwartzberg L, Kim ES, Liu D, Schrag D. Precision oncology: ໃຜ, ແນວໃດ, ຫຍັງ, ເວລາໃດ, ແລະເວລາໃດບໍ່?Am Soc Clin Oncol Educ Book.2017: 160-9.
23. Liu H, Meng X, Wang J. Realtime quantitative methylation
ການກວດຫາ gene PAX1 ໃນການກວດມະເຮັງປາກມົດລູກ.IntJ Gynecol ມະເຮັງ.2020;30:1488-92.
24. Imperiale TF, RansohoffDF, Itzkowitz SH, Levin TR, Lavin P, Lidgard GP, et al.ການທົດສອບ DNA multitargetstool ສໍາລັບການກວດຫາມະເຮັງລໍາໄສ້ໃຫຍ່.N EnglJ Med.ປີ 2014;370: 1287-97.
25. Li J, Li Y, Li W, Luo H, Xi Y, Dong S, et al.ການຈັດຕໍາແໜ່ງຄູ່ມື
ການຈັດລໍາດັບກໍານົດຮູບແບບ DNA methylation ທີ່ຜິດປົກກະຕິທີ່ປ່ຽນແປງຕົວຕົນຂອງເຊນແລະເຄືອຂ່າຍການເຝົ້າລະວັງ tumor-immune.ພັນທຸ ກຳ
Res.2019;29:270-80 .
26. Gao Q, LinYP, Li BS, Wang GQ, Dong LQ, Shen BY, et al.ການກວດຫາມະເຮັງຫຼາຍຊະນິດທີ່ບໍ່ໄດ້ລົບກວນໂດຍການໄຫຼວຽນຂອງລໍາດັບ DNA methylation ທີ່ບໍ່ມີຈຸລັງ (THUNDER): ການພັດທະນາແລະການສຶກສາການກວດສອບເອກະລາດ.Ann Oncol.2023;34:486-95.
27. Dong S, Li W, Wang L, Hu J, Song Y, Zhang B, et al.genes ທີ່ກ່ຽວຂ້ອງກັບ histone ແມ່ນ hypermethylated ໃນມະເຮັງປອດແລະ hypermethylated
HIST1H4F ສາມາດຮັບໃຊ້ biomarker ມະເຮັງກະເພາະອາຫານ.ມະເຮັງ2019;79:6101-12.
28. HeijnsdijkEA, Wever EM,AuvinenA, Hugosson J, Ciatto S, Nelen V, et al.ຜົນກະທົບດ້ານຄຸນນະພາບຂອງຊີວິດຂອງການກວດ antigen ສະເພາະຂອງຕ່ອມລູກໝາກ.N EnglJ Med.ປີ 2012;367:595-605.
29. LuzakA, Schnell-Inderst P, Bühn S, Mayer-Zitarosa A, Siebert U. ປະສິດທິພາບທາງດ້ານຄລີນິກຂອງການກວດ biomarker ການກວດຫາມະເຮັງທີ່ສະເໜີໃຫ້ເປັນການບໍລິການສຸຂະພາບທີ່ຈ່າຍເງິນດ້ວຍຕົນເອງ: ການທົບທວນຄືນລະບົບ.ສຸຂະພາບສາທາລະນະຂອງເອີໂຣ.ປີ 2016;26:498-505.
30. Dong S, Lu Q, Xu P, Chen L, Duan X, Mao Z, et al.
Hypermethylated PCDHGB7 ເປັນພຽງແຕ່ເຄື່ອງຫມາຍຂອງມະເຮັງທົ່ວໄປແລະການນໍາໃຊ້ຂອງມັນໃນການກວດສອບມະເຮັງປາກມົດລູກໃນຕອນຕົ້ນ.Clin Transl Med.2021;11: e457.
31. Yuan J, Mao Z, Lu Q, Xu P, Wang C, Xu X, et al.Hypermethylated PCDHGB7 ເປັນ biomarker ສໍາລັບການກວດພົບມະເຮັງ endometrial ໃນຕົວຢ່າງແປງ endometrial ແລະການຂູດປາກມົດລູກ.Front Mol Biosci.2022;8:774215.
32. Dong S, Yang Z, Xu P, Zheng W, Zhang B, Fu F, et al.ເຊິ່ງກັນແລະກັນ
ການດັດແກ້ epigenetic ສະເພາະໃນ SIX6 ທີ່ມີ hypermethylation ສໍາລັບຂັ້ນຕອນຂອງ precancerous ແລະການຕິດຕາມການເກີດ metastasis.ການສົ່ງສັນຍານເປົ້າຫມາຍ Ther.2022;7:208 .
33. Huang L, Guo Z, Wang F, Fu L. KRAS ການກາຍພັນ: ຈາກ undruggable ກັບ druggable ໃນມະເຮັງ.ການສົ່ງສັນຍານເປົ້າຫມາຍ Ther.2021;6:386 .
34. Belinsky SA, Nikula KJ, PalmisanoWA, MichelsR, SaccomannoG, GabrielsonE, et al.methylation Aberrant ຂອງ p16(INK4a) ແມ່ນເຫດການທີ່ເກີດຂື້ນໃນຕອນຕົ້ນຂອງມະເຮັງປອດແລະເປັນຕົວຊີ້ບອກທາງຊີວະພາບທີ່ມີທ່າແຮງສໍາລັບການວິນິດໄສເບື້ອງຕົ້ນ.Proc Natl Acad Sci USA.ປີ 1998;95:11891-6.
35. Robertson KD.DNA methylation ແລະພະຍາດຂອງມະນຸດ.Nat Rev Genet.2005;6:597-610.
36. WentzensenN, Walker JL, Gold MA, Smith KM, ZunaRE,
Mathews C, et al.ການກວດ biopsies ຫຼາຍຄັ້ງ ແລະການຊອກຄົ້ນຫາຄາຣະວາຂອງມະເຮັງປາກມົດລູກຢູ່ທີ່ colposcopy.J Clin Oncol.ປີ 2015;33:83-9 .
37. De Strooper LM, Meijer CJ, Berkhof J, Hesselink AT, Snijders
PJ, Steenbergen RD, et al.ການວິເຄາະ Methylation ຂອງ FAM19A4
gene ໃນ scrapes ປາກມົດລູກແມ່ນປະສິດທິພາບສູງໃນການກວດສອບປາກມົດລູກ
ມະເຮັງ ແລະ ບາດແຜ CIN2/3 ຂັ້ນສູງ.Cancer Prev Res (Phila).ປີ 2014;7:1251-7.
38. ໄທ AA, Solomon BJ, Sequist LV, Gainor JF, Heist RS.ມະເຮັງປອດ.Lancet.2021;398:535-54.
39. Grunnet M, Sorensen JB.Carcinoembryonic antigen (CEA) ເປັນເຄື່ອງໝາຍເນື້ອງອກໃນມະເຮັງປອດ.ມະເຮັງປອດ.ປີ 2012;76:138-43 .
40. Wood DE, KazerooniEA, Baum SL, EapenGA, EttingerDS, Hou L, et al.ການກວດຫາມະເຮັງປອດ, ເວີຊັ່ນ 3.2018, NCCN Clinical Practice Guidelines in Oncology.J Natl Compr Canc Netw.ປີ 2018;16:412-41.
41. ສະມາຄົມມະເຮັງອາເມຣິກາ.ຂໍ້ເທັດຈິງແລະຕົວເລກຂອງມະເຮັງ.Atlanta, GA, ສະຫະລັດອາເມລິກາ: ສະມາຄົມມະເຮັງອາເມລິກາ;2023 [ປັບປຸງ 2023 ມີນາ 1;ອ້າງເຖິງ 2023 ວັນທີ 22 ສິງຫາ].
42. FonthamETH, Wolf AMD, Church TR, EtzioniR, Flowers CR,
Herzig A, et al.ການກວດມະເຮັງປາກມົດລູກສຳລັບບຸກຄົນທີ່ມີຄວາມສ່ຽງໂດຍສະເລ່ຍ: ການປັບປຸງບົດແນະນຳປີ 2020 ຈາກສະມາຄົມມະເຮັງອາເມຣິກາ.CA Cancer J Clin.2020;70:321-46.
43. Clarke MA, Long BJ, Del Mar MorilloA, Arbyn M, Bakkum-Gamez JN, Wentzensen N. ສະມາຄົມຄວາມສ່ຽງຕໍ່ການເປັນມະເຮັງ endometrial ທີ່ມີເລືອດອອກຫຼັງຫມົດປະຈໍາເດືອນໃນແມ່ຍິງ: ການທົບທວນລະບົບແລະການວິເຄາະ meta.JAMA Intern Med.ປີ 2018;178:1210-22.
44. ຢາໂຄບ I, Gentry-MaharajA, Burnell M, ManchandaR, Singh N,
Sharma A, et al.ຄວາມອ່ອນໄຫວຂອງການກວດ ultrasound transvaginal
ສໍາລັບມະເຮັງ endometrial ໃນແມ່ຍິງ postmenopausal: ການສຶກສາການຄວບຄຸມກໍລະນີພາຍໃນກຸ່ມ UKCTOCS.Lancet Oncol.ປີ 2011;12:38-48 .
45. BabjukM, Burger M, CompératEM, Gontero P, MostafidAH,
PalouJ, et al.ສະມາຄົມເອີຣົບຂອງຄໍາແນະນໍາກ່ຽວກັບ Urology ກ່ຽວກັບມະເຮັງພົກຍ່ຽວທີ່ບໍ່ແມ່ນກ້າມເນື້ອ (TaT1 ແລະ Carcinoma In Situ) -
ອັບເດດ 2019.ເອີ ໂຣ.2019;76:639-57.
46. ອາຣົມ-ຊິງ ເຈບີ.ສິ່ງທ້າທາຍແລະຄວາມກ້າວຫນ້າໃນການວິນິດໄສ, ຊີວະວິທະຍາ, ແລະການປິ່ນປົວຂອງ urothelial tract ເທິງແລະ carcinomas ພົກຍ່ຽວ.Urol Oncol.ປີ 2017;35:462-4.
47. Rizvi S, KhanSA, Hallemeier CL, Kelley RK, Gores GJ.
Cholangiocarcinoma - ແນວຄວາມຄິດທີ່ພັດທະນາແລະຍຸດທະສາດການປິ່ນປົວ.Nat Rev Clin Oncol.ປີ 2018;15:95-111.
48. Ye Q, Ling S, Zheng S, Xu X. Liquid biopsy in hepatocellular
carcinoma: ແຜ່ກະຈາຍຈຸລັງ tumor ແລະ circulating tumor DNA.ມະເຮັງມໍ.2019;18:114 .
49. Zhang Y, Yao Y, Xu Y, Li L, Gong Y, Zhang K, et al.ມະເຮັງປາກມົດລູກ
ການກວດຫາເນື້ອງອກຂອງເນື້ອງອກຢູ່ໃນຄົນເຈັບຈີນຫຼາຍກວ່າ 10,000 ຄົນ.Nat Commun.2021;12:11 .
50. Eisenhauer EA, Therasse P, BogaertsJ, Schwartz LH, Sargent D, Ford R, et al.ເງື່ອນໄຂການປະເມີນຜົນການຕອບໂຕ້ໃຫມ່ໃນເນື້ອງອກແຂງ: ປັບປຸງຄໍາແນະນໍາ RECIST (ສະບັບ 1.1).ມະເຮັງເອີໂຣ.2009;45:228-47 .
51. LitièreS, Collette S, de Vries EG, Seymour L, BogaertsJ.RECIST - ການຮຽນຮູ້ຈາກອະດີດເພື່ອສ້າງອະນາຄົດ.Nat Rev Clin Oncol.
ປີ 2017;14:187-92.
52. Seymour L, BogaertsJ, Perrone A, FordR, Schwartz LH, Mandrekar S, et al.iRECIST: ຄໍາແນະນໍາສໍາລັບເງື່ອນໄຂການຕອບສະຫນອງສໍາລັບການນໍາໃຊ້ໃນການທົດລອງ
ການທົດສອບ immunotherapeutics.Lancet Oncol.ປີ 2017;18: e143-52.
53. PantelK, Alix-Panabières C. ການກວດເນື້ອເຍື່ອຂອງແຫຼວ ແລະພະຍາດທີ່ເຫຼືອໜ້ອຍທີ່ສຸດ - ຄວາມກ້າວໜ້າຫຼ້າສຸດ ແລະ ຜົນສະທ້ອນຕໍ່ການປິ່ນປົວ.Nat Rev Clin Oncol.2019;16:409-24 .
ອ້າງເຖິງບົດຄວາມນີ້ຄື: Qian C, Zou X, Li W, Li Y, Yu W. The outpost against cancer: universal cancer markers only.ມະເຮັງ Biol Med.2023;20:806-815.
doi: 10.20892/j.issn.2095-3941.2023.0313
ເວລາປະກາດ: 07-07-2024